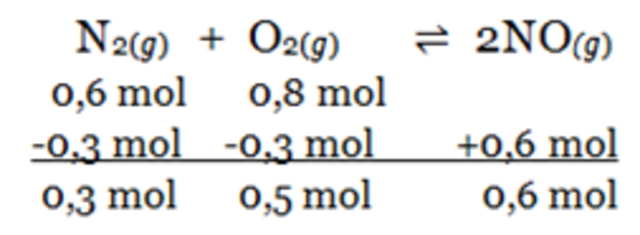Bank Soal Kimia SMA Reaksi Bolak-Balik dan Kesetimbangan Kimia
Soal
Soal Populer Hari Ini
Pecahan tersebut senilai dengan pecahan ...
Matematika
Level 4
Bilangan
Pecahan
Pecahan Senilai
Rumus untuk mencari keliling segitiga adalah ...
Matematika
Level 4
Geometri
Bangun Datar
Keliling dan Luas Segitiga
Ringkasan: Kaus Bau Si Mo Monyet

Buku yang berjudul "Kaus Bau Si Mo Monyet" karya David Bedford ini mengisahkan tentang si Mo monyet yang tidak mau mencuci kaus pelanginya, padahal sang ibu sudah mengingatkan agar Mo mencuci kausnya.
Mo selalu menggunakan kaus pelanginya untuk melakukan seluruh kegiatan mulai dari memetik buah beri, bermain lumpur dengan teman-temannya, membersihkan tangan sebelum makan, hingga membersihkan mulutnya setelah makan. Karena kaus Mo sangat kotor dan bau, ibu meminta agar kaus Mo dicuci terlebih dahulu. Namun, Mo menolaknya. Ibu memaksa Mo untuk membuka kausnya tetapi Mo tidak mau melepaskan kaus tersebut sehingga ibu dan Mo saling menarik kaus pelangi Mo. Setelah lama ditarik-tarik dengan bantuan teman Mo dan teman ibu, Mo mau mencuci kausnya. Setelah dicuci, Mo ingin memakai kembali kaus pelanginya. Tapi ternyata kaus tersebut melar karena ditarik-tarik, sehingga tidak bisa lagi dipakai di badannya. Agar tetap bisa menggunakan kaus pelanginya, Mo membuat ayunan dari kaus pelangi yang melar tersebut.
(Sumber: Erlangga for Kids)
Berdasarkan ringkasan di atas, suasana dalam buku cerita ini ....
Bahasa Indonesia
Level 4
Membaca
Buku Sastra
Meringkas Cerita Anak
Look at the picture and answer the question.

Source: freepik.com
What is his job?
Bahasa Inggris
Level 4
Bahasa Inggris
Jobs
Vocabulary: Jobs
Berikut ini yang merupakan bilangan kelipatan 4 adalah ...
Matematika
Level 4
Bilangan
Faktor dan Kelipatan
Kelipatan Bilangan
Poligon yang mempunyai 7 sisi dinamakan?
Matematika
Level 4
Geometri
Bangun Datar
Segi Banyak
KPK dari bilangan 12, 24, dan 90 adalah ....
Matematika
Level 4
Bilangan
FPB dan KPK
KPK
Cermati teks berikut!
Jaka Tarub

Suatu malam, Jaka Tarub bermimpi makan daging rusa yang lezat. Paginya Jaka Tarub pergi ke hutan untuk berburu rusa. Alih-alih rusa, yang ditemukan malah tujuh bidadari cantik yang sedang mandi di telaga. Dengan mengendap-endap, Jaka Tarub mengambil salah satu selendang bidadari yang ada di pinggir telaga. Karena tidak dapat pulang ke kahyangan tanpa selendangnya, Nawang Wulan terpaksa ditinggal oleh kakak-kakaknya.
Nawang Wulan yang bersedih hati karena ditinggal pun bersedia ikut Jaka Tarub pulang ke rumahnya. Tak lama kemudian, mereka pun menikah. Anak perempuan pertama mereka, Nawangsih, terlahir setelahnya. Sejak adanya Nawang Wulan dan Nawangsih, Jaka Tarub merasa hidupnya bahagia kembali.
Sejak pernikahannya dengan Nawang Wulan, Jaka Tarub merasakan adanya satu keanehan. Hal ini yaitu lumbung padinya tidak pernah berkurang meskipun selalu diambil berasnya untuk memasak nasi. Meski diminta berjanji untuk tidak mencari tahu, Jaka Tarub melanggar janjinya sendiri dengan mengintip periuk nasi yang sedang dimasak Nawang Wulan. Akibatnya, kekuatan Nawang Wulan pun hilang. Sejak itu ia harus menumbuk dan menampi beras seperti manusia lainnya. Akibatnya lumbung padi Jaka Tarub terus berkurang.
Suatu hari Nawang Wulan menemukan selendangnya yang sudah lama hilang di dalam lumbung. Nawang Wulan lalu memutuskan kembali ke kahyangan dengan selendangnya. Sebelum berangkat ke kahyangan, Nawang Wulan berpesan pada Jaka Tarub untuk meninggalkan Nawangsih di dekat rumahnya tiap malam. Setiap malam Nawang Wulan turun menghampiri Nawangsih dan kembali ke kahyangan menjelang pagi. Demikian hal ini terus berlanjut hingga Nawangsih beranjak dewasa. Setelahnya, Nawang Wulan tidak pernah lagi turun ke bumi dan Jaka Tarub tidak pernah bertemu dengannya lagi.
Tokoh yang berwatak licik pada cerita di atas adalah ....
Bahasa Indonesia
Level 4
Membaca
Teks Fiksi-Tokoh Cerita
Cerita Rakyat
Besar sudut terkecil yang terbentuk antara dua jarum jam pukul 04.30 adalah ...
Matematika
Level 4
Geometri
Garis dan Sudut
Sudut
Angka kecukupan gizi adalah pedoman kecukupan rata-rata zat gizi dalam sehari bagi seseorang.
Kandungan zat kalsium dalam segelas susu adalah 275 mg. Angka kecukupan gizi kalsium adalah 1.000 mg per harinya. Berarti segelas susu sudah mencukupi ... bagian dari angka kecukupan gizi kalsium.
Matematika
Level 4
Bilangan
Pecahan
Pecahan Senilai
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Pecahan tersebut senilai dengan pecahan ...
Rumus untuk mencari keliling segitiga adalah ...
Ringkasan: Kaus Bau Si Mo Monyet
Buku yang berjudul "Kaus Bau Si Mo Monyet" karya David Bedford ini mengisahkan tentang si Mo monyet yang tidak mau mencuci kaus pelanginya, padahal sang ibu sudah mengingatkan agar Mo mencuci kausnya.
Mo selalu menggunakan kaus pelanginya untuk melakukan seluruh kegiatan mulai dari memetik buah beri, bermain lumpur dengan teman-temannya, membersihkan tangan sebelum makan, hingga membersihkan mulutnya setelah makan. Karena kaus Mo sangat kotor dan bau, ibu meminta agar kaus Mo dicuci terlebih dahulu. Namun, Mo menolaknya. Ibu memaksa Mo untuk membuka kausnya tetapi Mo tidak mau melepaskan kaus tersebut sehingga ibu dan Mo saling menarik kaus pelangi Mo. Setelah lama ditarik-tarik dengan bantuan teman Mo dan teman ibu, Mo mau mencuci kausnya. Setelah dicuci, Mo ingin memakai kembali kaus pelanginya. Tapi ternyata kaus tersebut melar karena ditarik-tarik, sehingga tidak bisa lagi dipakai di badannya. Agar tetap bisa menggunakan kaus pelanginya, Mo membuat ayunan dari kaus pelangi yang melar tersebut.
(Sumber: Erlangga for Kids)
Berdasarkan ringkasan di atas, suasana dalam buku cerita ini ....
Look at the picture and answer the question.
Source: freepik.com
What is his job?
Berikut ini yang merupakan bilangan kelipatan 4 adalah ...
Poligon yang mempunyai 7 sisi dinamakan?
KPK dari bilangan 12, 24, dan 90 adalah ....
Cermati teks berikut!
Jaka Tarub
Suatu malam, Jaka Tarub bermimpi makan daging rusa yang lezat. Paginya Jaka Tarub pergi ke hutan untuk berburu rusa. Alih-alih rusa, yang ditemukan malah tujuh bidadari cantik yang sedang mandi di telaga. Dengan mengendap-endap, Jaka Tarub mengambil salah satu selendang bidadari yang ada di pinggir telaga. Karena tidak dapat pulang ke kahyangan tanpa selendangnya, Nawang Wulan terpaksa ditinggal oleh kakak-kakaknya.
Nawang Wulan yang bersedih hati karena ditinggal pun bersedia ikut Jaka Tarub pulang ke rumahnya. Tak lama kemudian, mereka pun menikah. Anak perempuan pertama mereka, Nawangsih, terlahir setelahnya. Sejak adanya Nawang Wulan dan Nawangsih, Jaka Tarub merasa hidupnya bahagia kembali.
Sejak pernikahannya dengan Nawang Wulan, Jaka Tarub merasakan adanya satu keanehan. Hal ini yaitu lumbung padinya tidak pernah berkurang meskipun selalu diambil berasnya untuk memasak nasi. Meski diminta berjanji untuk tidak mencari tahu, Jaka Tarub melanggar janjinya sendiri dengan mengintip periuk nasi yang sedang dimasak Nawang Wulan. Akibatnya, kekuatan Nawang Wulan pun hilang. Sejak itu ia harus menumbuk dan menampi beras seperti manusia lainnya. Akibatnya lumbung padi Jaka Tarub terus berkurang.
Suatu hari Nawang Wulan menemukan selendangnya yang sudah lama hilang di dalam lumbung. Nawang Wulan lalu memutuskan kembali ke kahyangan dengan selendangnya. Sebelum berangkat ke kahyangan, Nawang Wulan berpesan pada Jaka Tarub untuk meninggalkan Nawangsih di dekat rumahnya tiap malam. Setiap malam Nawang Wulan turun menghampiri Nawangsih dan kembali ke kahyangan menjelang pagi. Demikian hal ini terus berlanjut hingga Nawangsih beranjak dewasa. Setelahnya, Nawang Wulan tidak pernah lagi turun ke bumi dan Jaka Tarub tidak pernah bertemu dengannya lagi.
Tokoh yang berwatak licik pada cerita di atas adalah ....
Besar sudut terkecil yang terbentuk antara dua jarum jam pukul 04.30 adalah ...
Angka kecukupan gizi adalah pedoman kecukupan rata-rata zat gizi dalam sehari bagi seseorang.
Kandungan zat kalsium dalam segelas susu adalah 275 mg. Angka kecukupan gizi kalsium adalah 1.000 mg per harinya. Berarti segelas susu sudah mencukupi ... bagian dari angka kecukupan gizi kalsium.