Bank Soal Kimia SMA Sel Elektrolisis dan Perhitungannya
Soal
Soal Populer Hari Ini
Hasil dari adalah ....
Matematika
Level 5
Bilangan
Operasi Hitung Pecahan
Operasi Hitung Berbagai Bentuk Pecahan

Andi mengikuti lomba menulis cerpen dalam iklan tersebut. Jika Andi berhasil menjadi juara II, hadiah yang berhasil didapatkan Andi adalah sertifikat dan uang sebesar ....
Bahasa Indonesia
Level 5
Membaca
Iklan
Identifikasi Informasi
Ciri yang menunjukkan Indonesia sebagai negara maritim adalah ....
IPS
Level 5
Geografi
Karakteristik Geografi Wilayah Indonesia
Karakteristik Geografis
Read the text below. Then, fill in the blank with a correct verb to be.

Source: creazilla.com
My name is Claire. I live in Arizona. I am in fifth grade. I have a brother. His name is Peter. He is in fourth grade.
Based on the text, we know that Claire and Peter ... students.
Bahasa Inggris
Level 5
Bahasa Inggris
Friendship
Self-Introduction
Sebuah bak mandi terisi air sebanyak 1.500 liter. Agar bak tersebut dapat terisi 2 m3 air, maka volume bak harus ditambah sebanyak … m3.
Matematika
Level 5
Geometri
Perbandingan Dua Besaran
Debit
Perhatikan gambar!
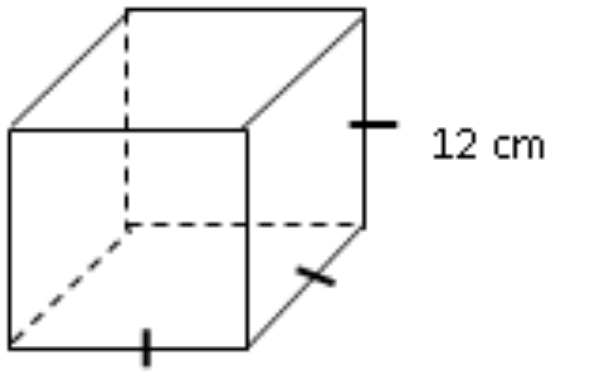
Mira akan membungkus kado yang berbentuk kubus seperti gambar. Luas kertas kado minimal yang dibutuhkan Mira adalah ....
Matematika
Level 5
Geometri
Balok dan Kubus
Luas Permukaan Balok dan Kubus
Perhatikan gambar berikut ini!
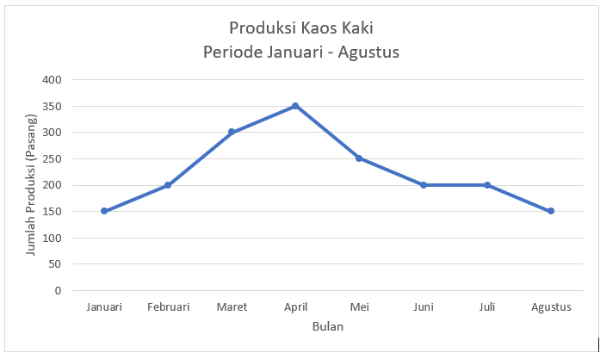
Hasil produksi kaos kaki terbanyak terjadi pada bulan ...
Matematika
Level 5
Statistika
Pengumpulan dan Penyajian Data
Membaca Data
Perhatikan pernyataan berikut!
- Berikan informasi tambahan atau deretan penjelas tentang pernyataan umum yang sudah disampaikan pada paragraf sebelumnya.
- Tentukan hal pokok yang akan dibahas.
- Berikan kesimpulan tentang hal yang sudah dibahas berdasarkan pernyataan umum dan deretan penjelas.
- Kembangkan deretan penjelas menjadi beberapa paragraf.
- Cari informasi sebanyak-banyaknya tentang hal yang ingin dibahas.
- Buatlah pernyataan umum tentang hal yang ingin dibahas.
Urutan langkah yang tepat dalam menulis teks eksplanasi yaitu ....
Bahasa Indonesia
Level 5
Membaca
Teks Eksplanasi
Struktur Teks Eksplanasi
Perhatikan diagram berikut!

Pernyataan yang sesuai dengan diagram di atas adalah ...
Matematika
Level 5
Statistika
Pengumpulan dan Penyajian Data
Membaca Data
Bacalah kutipan surat undangan berikut ini!
Dengan hormat,
Melalui surat ini, kami bermaksud mengundang Bapak/Ibu untuk hadir dalam acara pengambilan rapor semester ganjil untuk kelas I-VI tahun pelajaran 2019/2020. Acara tersebut akan dilaksanakan pada:
hari : Sabtu
tanggal : 7 Desember 2019
waktu : 09.00 WIB
tempat : Kelas masing-masing
Kami harap Bapak/Ibu dapat hadir tepat waktu. [...]
Kalimat efektif yang tepat untuk melengkapi kutipan surat undangan tersebut adalah ....
Bahasa Indonesia
Level 5
Membaca
Surat Undangan
Menulis Surat Undangan
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Hasil dari adalah ....
Andi mengikuti lomba menulis cerpen dalam iklan tersebut. Jika Andi berhasil menjadi juara II, hadiah yang berhasil didapatkan Andi adalah sertifikat dan uang sebesar ....
Ciri yang menunjukkan Indonesia sebagai negara maritim adalah ....
Read the text below. Then, fill in the blank with a correct verb to be.

Source: creazilla.com
My name is Claire. I live in Arizona. I am in fifth grade. I have a brother. His name is Peter. He is in fourth grade.
Based on the text, we know that Claire and Peter ... students.
Sebuah bak mandi terisi air sebanyak 1.500 liter. Agar bak tersebut dapat terisi 2 m3 air, maka volume bak harus ditambah sebanyak … m3.
Perhatikan gambar!
Mira akan membungkus kado yang berbentuk kubus seperti gambar. Luas kertas kado minimal yang dibutuhkan Mira adalah ....
Perhatikan gambar berikut ini!
Hasil produksi kaos kaki terbanyak terjadi pada bulan ...
Perhatikan pernyataan berikut!
- Berikan informasi tambahan atau deretan penjelas tentang pernyataan umum yang sudah disampaikan pada paragraf sebelumnya.
- Tentukan hal pokok yang akan dibahas.
- Berikan kesimpulan tentang hal yang sudah dibahas berdasarkan pernyataan umum dan deretan penjelas.
- Kembangkan deretan penjelas menjadi beberapa paragraf.
- Cari informasi sebanyak-banyaknya tentang hal yang ingin dibahas.
- Buatlah pernyataan umum tentang hal yang ingin dibahas.
Urutan langkah yang tepat dalam menulis teks eksplanasi yaitu ....
Perhatikan diagram berikut!
Pernyataan yang sesuai dengan diagram di atas adalah ...
Bacalah kutipan surat undangan berikut ini!
Dengan hormat,
Melalui surat ini, kami bermaksud mengundang Bapak/Ibu untuk hadir dalam acara pengambilan rapor semester ganjil untuk kelas I-VI tahun pelajaran 2019/2020. Acara tersebut akan dilaksanakan pada:
hari : Sabtu tanggal : 7 Desember 2019 waktu : 09.00 WIB tempat : Kelas masing-masing
Kami harap Bapak/Ibu dapat hadir tepat waktu. [...]
Kalimat efektif yang tepat untuk melengkapi kutipan surat undangan tersebut adalah ....







