Bank Soal Kimia SMA Konsep Kelarutan dan Hasil Kali Kelarutan
Soal
Soal Populer Hari Ini
Sebuah dadu dilempar 30 kali. Frekuensi harapan muncul mata dadu bilangan prima ganjil adalah...
Matematika
Level 8
Statistika
Peluang
Berikut manakah yang merupakan rumus mencari luas lingkaran?
Matematika
Level 8
Geometri
Lingkaran
Luas dan Keliling Lingkaran
Perhatikan gambar berikut!
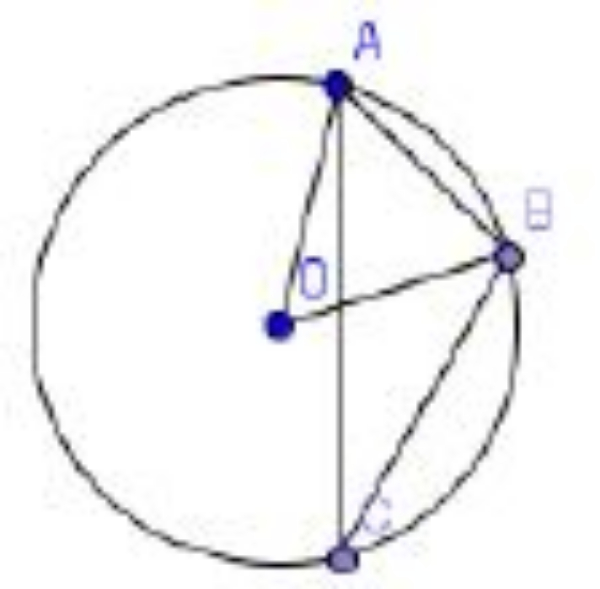
Jika sudut ABO = 55o, hitunglah besar sudut ACB!
Matematika
Level 8
Geometri
Lingkaran
Manakah di antara koordinat titik berikut yang terletak di kuadran IV?
Matematika
Level 8
Geometri
Koordinat Kartesius
Syarat informasi yang layak diangkat menjadi sebuah berita adalah memiliki sifat ....
Bahasa Indonesia
Level 8
Menulis
Teks Berita
Simpulan Isi Berita
Andy — study — hard — Kate
Which comparative sentence is correct based on the clues above?
Bahasa Inggris
Level 8
Bahasa Inggris
Comparisons of people or things
Degrees of Comparison of Adverbs
Titik A berjarak 8 satuan di sebelah kiri sumbu-Y dan berada di atas sumbu-X dengan jarak setengah dari jaraknya terhadap sumbu-Y.
Berapakah koordinat letak titik A?
Matematika
Level 8
Geometri
Koordinat Kartesius
Koordinat Posisi Suatu Benda
Persamaan bunyi yang terdapat pada akhir bait sebuah puisi yang dibuat oleh penyair agar puisi semakin indah disebut dengan ....
Bahasa Indonesia
Level 8
Menulis
Puisi
Unsur-unsur puisi
Kedai Minuman Rina
Rina akan membuka kedai minuman kekinian minggu depan. Ia membuat poster untuk mempromosikan kedai tersebut. Perhatikan poster kedai minuman milik Rina di bawah ini!

(Sumber Gambar: foodyas.com)
Di mana kamu bisa mendapatkan informasi lebih lanjut tentang kedai minuman milik Rina?
Bahasa Indonesia
Level 8
Menulis
Iklan, Slogan, Poster
Read the dialogue carefully.

Picture: today.line.me
Rossa : Do you know Tiara Anugrah?
Yoga : Yes. She is a singer, right? She can sing various genres of song very well.
Rossa : Yes. I envy her. Can you sing?
Yoga : Are you joking? Of course I can't. How about you?
Rossa : I can sing particular songs. But I can't perform them well.
Yoga : Why?
Rossa : My voice isn't good enough.
"I can sing particular songs." (Rossa, line 5)
The word particular has similar meaning with ....
Bahasa Inggris
Level 8
Bahasa Inggris
Interaction among students inside and outside classrooms
Expressions of Explaining Abilities
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Sebuah dadu dilempar 30 kali. Frekuensi harapan muncul mata dadu bilangan prima ganjil adalah...
Berikut manakah yang merupakan rumus mencari luas lingkaran?
Perhatikan gambar berikut!
Jika sudut ABO = 55o, hitunglah besar sudut ACB!
Manakah di antara koordinat titik berikut yang terletak di kuadran IV?
Syarat informasi yang layak diangkat menjadi sebuah berita adalah memiliki sifat ....
Andy — study — hard — Kate
Which comparative sentence is correct based on the clues above?
Titik A berjarak 8 satuan di sebelah kiri sumbu-Y dan berada di atas sumbu-X dengan jarak setengah dari jaraknya terhadap sumbu-Y.
Berapakah koordinat letak titik A?
Persamaan bunyi yang terdapat pada akhir bait sebuah puisi yang dibuat oleh penyair agar puisi semakin indah disebut dengan ....
Kedai Minuman Rina
Rina akan membuka kedai minuman kekinian minggu depan. Ia membuat poster untuk mempromosikan kedai tersebut. Perhatikan poster kedai minuman milik Rina di bawah ini!
(Sumber Gambar: foodyas.com)
Di mana kamu bisa mendapatkan informasi lebih lanjut tentang kedai minuman milik Rina?
Read the dialogue carefully.
Picture: today.line.me
Rossa : Do you know Tiara Anugrah? Yoga : Yes. She is a singer, right? She can sing various genres of song very well. Rossa : Yes. I envy her. Can you sing? Yoga : Are you joking? Of course I can't. How about you? Rossa : I can sing particular songs. But I can't perform them well. Yoga : Why? Rossa : My voice isn't good enough.
"I can sing particular songs." (Rossa, line 5)
The word particular has similar meaning with ....







