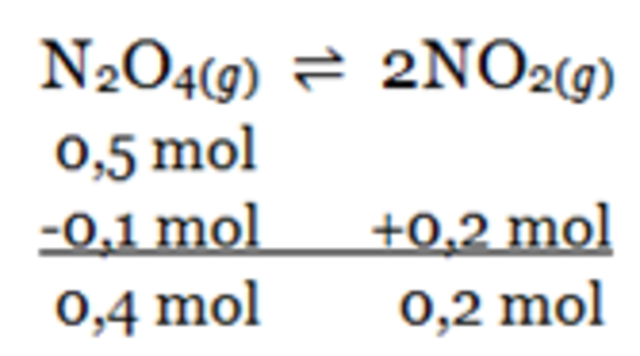Bank Soal Kimia SMA Reaksi Bolak-Balik dan Kesetimbangan Kimia
Soal
Soal Populer Hari Ini
Perhatikan tingkat organisasi kehidupan berikut!
- Jaringan
- Sel
- Populasi
- Organ
- Individu
Urutan tingkat organisasi kehidupan mulai dari yang sederhana ke kompleks adalah ....
Biologi
Level 10
Biologi
Ruang Lingkup Biologi
Objek dan Permasalahan Biologi
To support her friend, Amy gives a complement to Kelly by saying ...
Bahasa Inggris
Level 10
Congratulating and Complimenting
Expressions of Congratulating and Complimenting
Setelah melakukan percobaan mengenai ayunan sederhana, data berupa panjang tali, massa bandul, jumlah getaran, dan waktu dihitung menggunakan rumus. Selanjutnya hasil perhitungan akan dibandingkan dengan teori apakah hasilnya sesuai atau tidak. Proses ini merupakan metode ilmiah tahap ....
Fisika
Level 10
Fisika
Hakikat Fisika dan Keselamatan Kerja Laboratorium
Hakikat dan Peran Fisika
Berikut penulisan nama spesies yang benar menurut tata nama binomial adalah ....
Biologi
Level 10
Biologi
Keanekaragaman Hayati
Klasifikasi Makhluk Hidup
Nilai pada persamaan adalah ....
Matematika
Level 10
Aljabar
Persamaan dan Pertidaksamaan Nilai Mutlak
Persamaan Linear Satu Variabel
Film Dilan: 1990 menjadi salah satu film Indonesia dengan jumlah penonton terbanyak.
Penulisan judul film yang benar adalah ….
Bahasa Indonesia
Level 10
Teks Laporan Hasil Observasi
Menulis Teks Laporan Hasil Observasi
Ilmu yang mempelajari hubungan timbal balik antara makhluk hidup dan lingkungannya di dalam suatu ekosistem disebut dengan istilah ....
Biologi
Level 10
Biologi
Ekologi
Ekologi dan Komponen Ekosistem
Pertidaksamaan yang tepat untuk daerah penyelesaian di bawah ini adalah ....

Matematika
Level 10
Aljabar
Sistem Pertidaksamaan Dua Variabel
Pertidaksamaan Dua Variabel
Perhatikan gambar berikut!
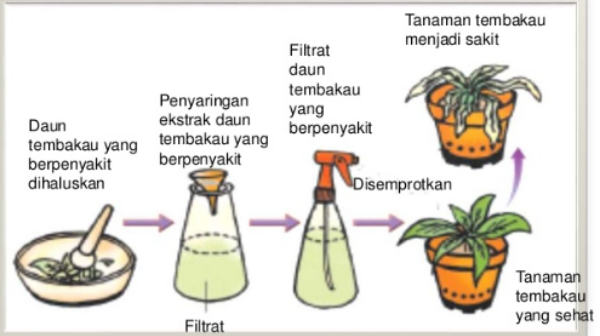
sumber: sucsload.blogspot.com
Penelitian pada tembakau seperti gambar di atas dilakukan oleh ....
Biologi
Level 10
Biologi
Virus
Sejarah Virus
Dalam melaksanakan metode ilmiah, terkadang kesimpulan yang didapatkan tidaklah sesuai dengan hipotesis awal yang telah dibuat. Untuk itu, hal yang harus dilakukan adalah ....
Kimia
Level 10
Perkenalan Ilmu Kimia
Metode Ilmiah dan Laboratorium Kimia
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Perhatikan tingkat organisasi kehidupan berikut!
- Jaringan
- Sel
- Populasi
- Organ
- Individu
Urutan tingkat organisasi kehidupan mulai dari yang sederhana ke kompleks adalah ....
To support her friend, Amy gives a complement to Kelly by saying ...
Setelah melakukan percobaan mengenai ayunan sederhana, data berupa panjang tali, massa bandul, jumlah getaran, dan waktu dihitung menggunakan rumus. Selanjutnya hasil perhitungan akan dibandingkan dengan teori apakah hasilnya sesuai atau tidak. Proses ini merupakan metode ilmiah tahap ....
Berikut penulisan nama spesies yang benar menurut tata nama binomial adalah ....
Nilai pada persamaan adalah ....
Film Dilan: 1990 menjadi salah satu film Indonesia dengan jumlah penonton terbanyak.
Penulisan judul film yang benar adalah ….
Ilmu yang mempelajari hubungan timbal balik antara makhluk hidup dan lingkungannya di dalam suatu ekosistem disebut dengan istilah ....
Pertidaksamaan yang tepat untuk daerah penyelesaian di bawah ini adalah ....
Perhatikan gambar berikut!
sumber: sucsload.blogspot.com
Penelitian pada tembakau seperti gambar di atas dilakukan oleh ....
Dalam melaksanakan metode ilmiah, terkadang kesimpulan yang didapatkan tidaklah sesuai dengan hipotesis awal yang telah dibuat. Untuk itu, hal yang harus dilakukan adalah ....