Bank Soal Kimia SMA Konsentrasi Ion dalam Larutan Asam dan Basa
Soal
Soal Populer Hari Ini
Dalam percobaan pengetosan dua koin, banyaknya ruang sampel yang terjadi yaitu ....
Matematika
Level 8
Statistika
Peluang
Kakak mempunyai tali berbentuk lingkaran dengan panjang jari-jari 7 cm, sedangkan adik mempunyai tali berbentuk lingkaran dengan panjang jari-jari 3,5 cm. Perbandingan panjang tali kakak terhadap adik adalah ...
Matematika
Level 8
Geometri
Lingkaran
Luas dan Keliling Lingkaran
Perhatikan gambar berikut!
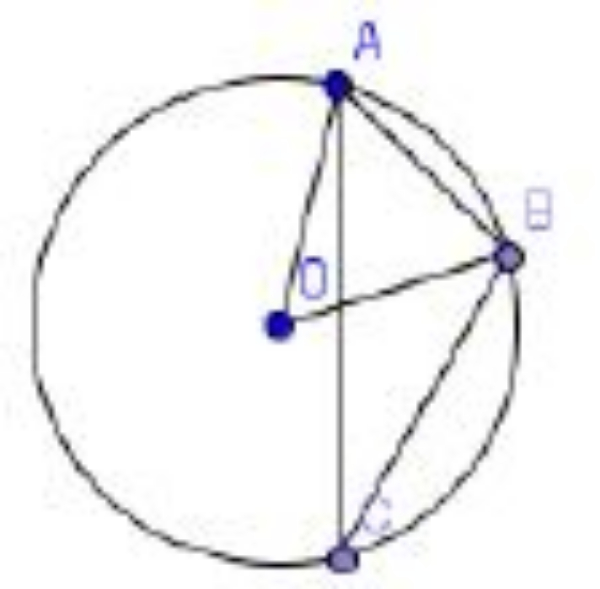
Jika sudut ABO = 55o, hitunglah besar sudut ACB!
Matematika
Level 8
Geometri
Lingkaran
Apabila jarak yang terbentuk antara titik G( i, -11) dengan titik F(18, -4) adalah satuan, berapakah nilai i ?
Matematika
Level 8
Geometri
Koordinat Kartesius
Perhatikan teks berita berikut.
Tiga Dosa di Sekolah yang Tidak Bisa Ditoleransi
Menteri Pendidikan dan Kebudayaan, Nadiem Makariem, menuturkan bahwa ada tiga dosa di sekolah yang tidak bisa ditoleransi. Ketiga dosa tersebut adalah intoleransi, kekerasan seksual, dan perundungan. Menurutnya, ketiga dosa tersebut harus ditindak tegas supaya tidak terus berulang.
Salah satu upaya yang dilakukan pemerintah untuk mengatasi permasalahan tersebut adalah dengan meluncurkan buku pedoman antikekerasan. Peluncuran buku tersebut dilakukan pada acara webinar dalam rangka memperingati Hari Anak Universal. Selain itu, pemerintah juga menyelenggarakan program Sekolah Ramah Anak untuk menjaga keamanan dan kenyamanan.
(Sumber: kompas.com dengan penyesuaian)
Tanggapan yang sesuai untuk teks berita tersebut adalah …
Bahasa Indonesia
Level 8
Menulis
Teks Berita
Menulis Teks Berita
Read the following comments of a broadway show.

Template/source: canva.com, linetv.com
Whose comment uses a comparative adverb?
Bahasa Inggris
Level 8
Bahasa Inggris
Comparisons of people or things
Degrees of Comparison of Adverbs
Segitiga siku-siku SRQ digambar pada bidang koordinat sebagai berikut :
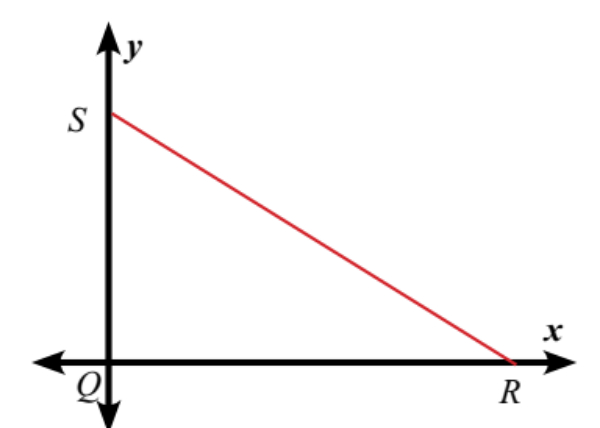
Jika panjang QR adalah 7 satuan dan panjang QS adalah 5 satuan, maka titik-titik koordinat Q, R, dan S secara berurutan adalah?
Matematika
Level 8
Geometri
Koordinat Kartesius
Posisi Titik terhadap Titik Tertentu
Bacalah puisi di bawah ini!
Kau
Lihat kami!
Kami mencoba kuat diatas kekurangan
Tak lelah banting tulang
Tapi kau?
Lihat dirimu!
Kau tak bersyukur dengan dirimu
Kau curi hak kami
Kau biarkan kami menderita
Tapi kau?
Seakan menari-nari diatas penderitaan kami
Lihat kami!
Apa tak kau lihat keringat kami?
Keletihan kami
Hanya demi sesuap nasi
Lihat negeri ini!
Sudah tiadakah hati?
Sudah tiadakah mata?
Hingga tak pernah kau lihat kami
Lalu, harus kemanakah kami?
Kami memang tak mampu balas dirimu
Karena Tuhan yang akan balas dirimu
(Karya: Nuke Hanasasmit)
Puisi di atas termasuk jenis puisi ....
Bahasa Indonesia
Level 8
Menulis
Puisi
Unsur-unsur puisi
Perhatikan gambar berikut!

Apa pesan yang disampaikan dalam iklan tersebut?
Bahasa Indonesia
Level 8
Menulis
Iklan, Slogan, Poster
Simpulan Isi Iklan, Slogan, Poster
Mention the ability of the following profession.

Source: pngtime.com
What is the best expression to show his ability?
Bahasa Inggris
Level 8
Bahasa Inggris
Interaction among students inside and outside classrooms
Expressions of Explaining Abilities
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Dalam percobaan pengetosan dua koin, banyaknya ruang sampel yang terjadi yaitu ....
Kakak mempunyai tali berbentuk lingkaran dengan panjang jari-jari 7 cm, sedangkan adik mempunyai tali berbentuk lingkaran dengan panjang jari-jari 3,5 cm. Perbandingan panjang tali kakak terhadap adik adalah ...
Perhatikan gambar berikut!
Jika sudut ABO = 55o, hitunglah besar sudut ACB!
Apabila jarak yang terbentuk antara titik G( i, -11) dengan titik F(18, -4) adalah satuan, berapakah nilai i ?
Perhatikan teks berita berikut.
Tiga Dosa di Sekolah yang Tidak Bisa Ditoleransi
Menteri Pendidikan dan Kebudayaan, Nadiem Makariem, menuturkan bahwa ada tiga dosa di sekolah yang tidak bisa ditoleransi. Ketiga dosa tersebut adalah intoleransi, kekerasan seksual, dan perundungan. Menurutnya, ketiga dosa tersebut harus ditindak tegas supaya tidak terus berulang.
Salah satu upaya yang dilakukan pemerintah untuk mengatasi permasalahan tersebut adalah dengan meluncurkan buku pedoman antikekerasan. Peluncuran buku tersebut dilakukan pada acara webinar dalam rangka memperingati Hari Anak Universal. Selain itu, pemerintah juga menyelenggarakan program Sekolah Ramah Anak untuk menjaga keamanan dan kenyamanan.
(Sumber: kompas.com dengan penyesuaian)
Tanggapan yang sesuai untuk teks berita tersebut adalah …
Read the following comments of a broadway show.
Template/source: canva.com, linetv.com
Whose comment uses a comparative adverb?
Segitiga siku-siku SRQ digambar pada bidang koordinat sebagai berikut :
Jika panjang QR adalah 7 satuan dan panjang QS adalah 5 satuan, maka titik-titik koordinat Q, R, dan S secara berurutan adalah?
Bacalah puisi di bawah ini!
Kau
Lihat kami!
Kami mencoba kuat diatas kekurangan
Tak lelah banting tulang
Tapi kau?
Lihat dirimu!
Kau tak bersyukur dengan dirimu
Kau curi hak kami
Kau biarkan kami menderita
Tapi kau?
Seakan menari-nari diatas penderitaan kami
Lihat kami!
Apa tak kau lihat keringat kami?
Keletihan kami
Hanya demi sesuap nasi
Lihat negeri ini!
Sudah tiadakah hati?
Sudah tiadakah mata?
Hingga tak pernah kau lihat kami
Lalu, harus kemanakah kami?
Kami memang tak mampu balas dirimu
Karena Tuhan yang akan balas dirimu
(Karya: Nuke Hanasasmit)
Puisi di atas termasuk jenis puisi ....
Perhatikan gambar berikut!
Apa pesan yang disampaikan dalam iklan tersebut?
Mention the ability of the following profession.
Source: pngtime.com
What is the best expression to show his ability?







