Bank Soal Kimia SMA Sel Volta dan Potensial Elektrode Standar
Soal
Memahami LOTS
Soal Populer Hari Ini
Hasil dari berupa ...
Matematika
Level 6
Bilangan
Operasi Hitung Bilangan Bulat dan Pecahan
Operasi Hitung Bilangan Bulat
Complete the sentence below.

Because the weather was nice, Rino ________.
Bahasa Inggris
Level 6
Bahasa Inggris
Past Holidays
Recount Text
Kalimat tanya yang sesuai untuk menanyakan informasi pada kalimat ketiga paragraf pertama adalah ….
Bahasa Indonesia
Level 6
Membaca
Buku Sejarah
Menggali Informasi (5W+1H)
Sebuah kerucut mempunyai jari-jari alas 14 cm dan tinggi 15 cm. Volume kerucut tersebut adalah ... cm3.
Matematika
Level 6
Geometri
Bangun Ruang
Volume dan Luas Permukaan Bangun Ruang
Hasil dari , nilai adalah ...
Matematika
Level 6
Bilangan
Operasi Hitung Bilangan Bulat dan Pecahan
Operasi Hitung Bilangan Bulat
Perhatikan gambar berikut!
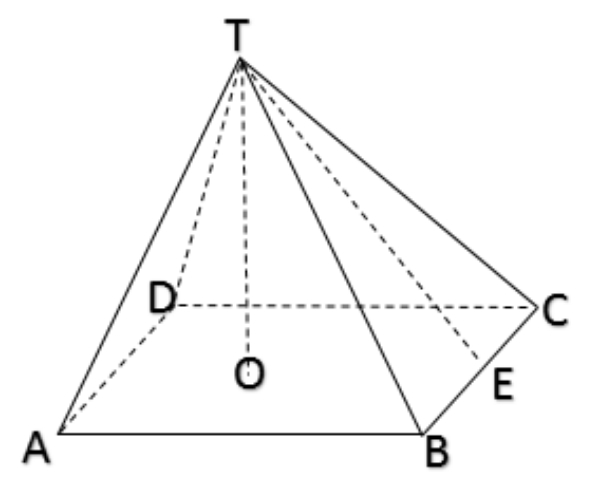
Jika AB = 16 cm, BC = 20 cm, TO = 6 cm, TE =10 cm, dan tinggi semua sisi tegak adalah sama, maka luas permukaan bangun limas di atas adalah ... cm2.
Matematika
Level 6
Geometri
Bangun Ruang
Volume dan Luas Permukaan Bangun Ruang
Yang perlu dicantumkan dalam laporan hasil pengamatan adalah ….
Bahasa Indonesia
Level 6
Menulis
Teks Laporan Hasil Pengamatan
Menulis Teks Laporan
Suhu udara di sebuah ruang adalah 0C. Setiap jam mengalami kenaikan suhu sebesar 20C. Suhu ruangan tersebut setelah 3 jam sebesar ... 0C
Bunga yang memiliki benang sari dan putik sekaligus dalam satu bunga disebut sebagai ....
IPA
Level 6
Biologi
Perkembangbiakan Makhluk Hidup
Perkembangbiakan Tumbuhan
Saya ucapkan terima kasih karena telah memberikan kesempatan kepada saya untuk berpidato pada kesempatan kali ini. Pada kesempatan kali ini, saya akan menyampaikan pentingnya menjaga kebersihan kelas.
Penggalan teks pidato tersebut merupakan bagian ….
Bahasa Indonesia
Level 6
Membaca
Teks Pidato
Menggali Isi
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Hasil dari berupa ...
Complete the sentence below.

Because the weather was nice, Rino ________.
Kalimat tanya yang sesuai untuk menanyakan informasi pada kalimat ketiga paragraf pertama adalah ….
Sebuah kerucut mempunyai jari-jari alas 14 cm dan tinggi 15 cm. Volume kerucut tersebut adalah ... cm3.
Hasil dari , nilai adalah ...
Perhatikan gambar berikut!
Jika AB = 16 cm, BC = 20 cm, TO = 6 cm, TE =10 cm, dan tinggi semua sisi tegak adalah sama, maka luas permukaan bangun limas di atas adalah ... cm2.
Yang perlu dicantumkan dalam laporan hasil pengamatan adalah ….
Suhu udara di sebuah ruang adalah 0C. Setiap jam mengalami kenaikan suhu sebesar 20C. Suhu ruangan tersebut setelah 3 jam sebesar ... 0C
Bunga yang memiliki benang sari dan putik sekaligus dalam satu bunga disebut sebagai ....
Saya ucapkan terima kasih karena telah memberikan kesempatan kepada saya untuk berpidato pada kesempatan kali ini. Pada kesempatan kali ini, saya akan menyampaikan pentingnya menjaga kebersihan kelas.
Penggalan teks pidato tersebut merupakan bagian ….







