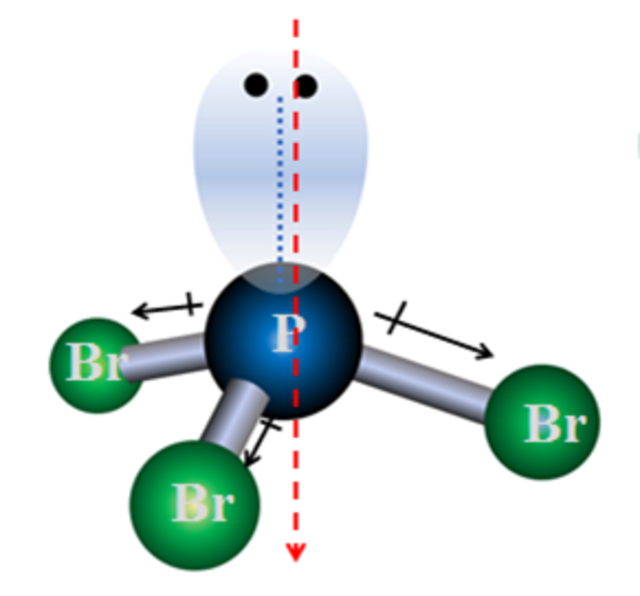
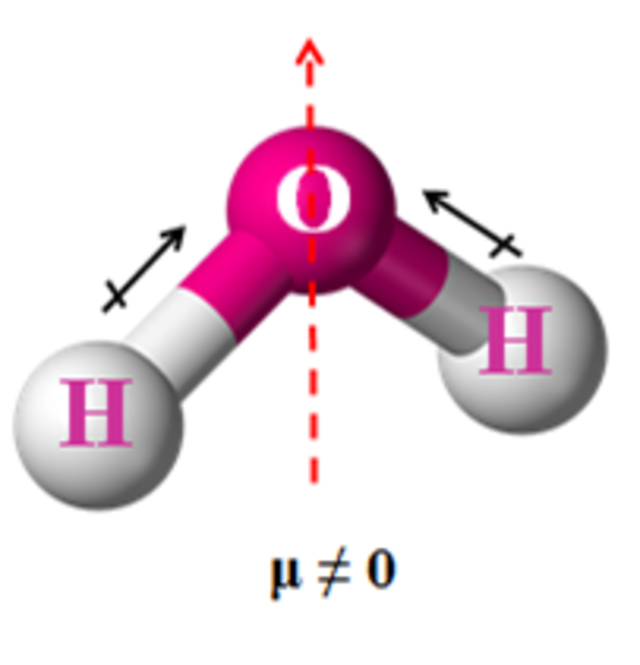
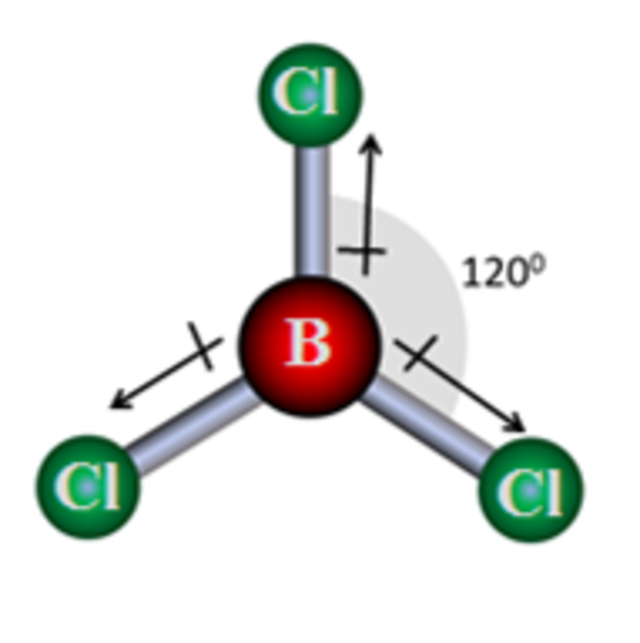
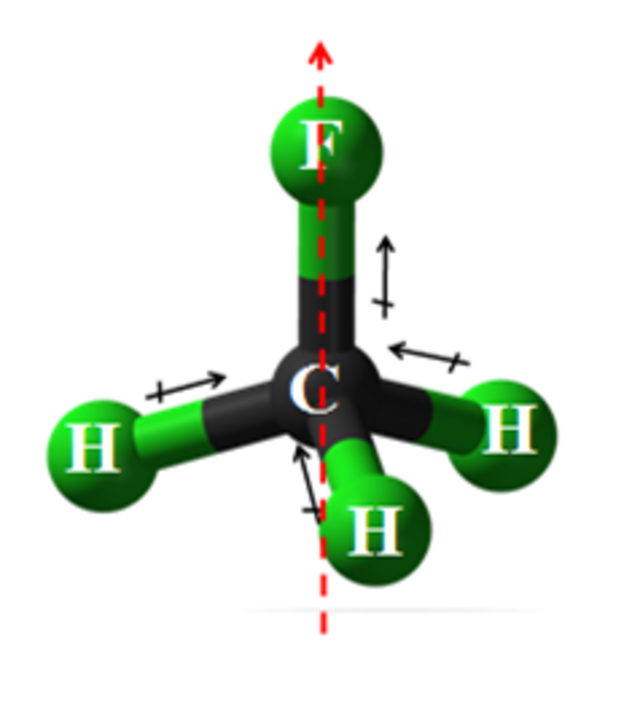
Bank Soal Kimia SMA Memprediksi Bentuk Molekul
Soal
Memahami LOTS
Soal Populer Hari Ini
Keliling sebuah persegi panjang sama dengan keliling sebuah persegi. Lebar persegi panjang lebih pendek 8 cm daripada panjangnya. Jika sisi persegi dapat diketahui dari persamaan: 5(s + 16) = 180, di mana s adalah sisi persegi, maka pernyataan berikut yang benar adalah ...
Matematika
Level 7
Aljabar
Persamaan dan Pertidaksamaan Linear Satu Variabel
Persamaan Linear Satu Variabel (PLSV)
= ...
Matematika
Level 7
Bilangan
Bilangan dan Operasi Hitung Bilangan
Bilangan Berpangkat



Perhatikan gambar di atas. Gambar itu disebut …
Matematika
Level 7
Bilangan
Himpunan
Konsep dan Macam-Macam Himpunan
Diketahui dua garis sejajar yang dipotong oleh sebuah garis lain. Pasangan sudut yang memiliki jumlah 180o adalah ....
Matematika
Level 7
Geometri
Garis dan Sudut
Hubungan Antar Sudut
Berikut ini yang tidak terdapat pada bagian identifikasi teks deskripsi adalah ….
Bahasa Indonesia
Level 7
Menulis
Teks Deskripsi
Struktur dan Kebahasaan Teks Deskripsi
Hasil dari
Matematika
Level 7
Aljabar
Bentuk Aljabar
Operasi Hitung Bentuk Aljabar
Cermati kutipan surat berikut ini.

Berdasarkan isi surat di atas, sifat si pengirim dulu waktu di sekolah adalah ....
Bahasa Indonesia
Level 7
Menulis
Surat Pribadi dan Surat Dinas
Simpulan Isi Surat Pribadi dan Surat Dinas
Perhatikan penggalan buku fiksi berikut.
Hiruk pikuk bunyi kendaraan mulai memecahkan keheningan pagi. Jalan Veteran mulai ramai dipenuhi angkutan kota yang lalu-lalang. Ada yang pergi bekerja, ada yang hanya sekadar berjalan-jalan pagi. Ada yang ingin berangkat sekolah. Semuanya terlihat terburu-buru.
(Dikutip dari novel Origami Hati karya Boy Candra)
Unsur yang menonjol pada penggalan buku fiksi tersebut adalah ….
Bahasa Indonesia
Level 7
Menulis
Buku Fiksi dan Nonfiksi
Unsur Pembangun Buku Fiksi dan Nonfiksi
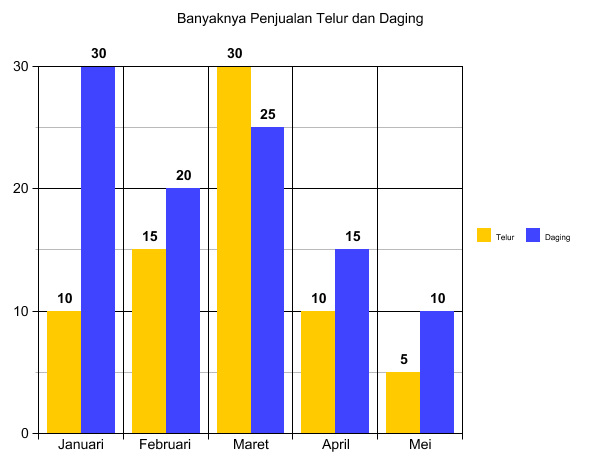
Kenaikan penjualan telur tertinggi terjadi pada bulan ....
Matematika
Level 7
Statistika
Penyajian dan Pengolahan Data
Penyajian dan Pengolahan Data
Read the dialogue below and answer the question.
Pita : Hai, Marel. Can I ask you something?
Marrel: Sure, what is it?
Pita : Is your name spelled M-A-R-E-L?
Marrel: No, It should be M-A-R-R-E-L.
Pita asks Marrel because she wants to know ....
Bahasa Inggris
Level 7
Bahasa Inggris
Describing oneself
Self Introduction
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Keliling sebuah persegi panjang sama dengan keliling sebuah persegi. Lebar persegi panjang lebih pendek 8 cm daripada panjangnya. Jika sisi persegi dapat diketahui dari persamaan: 5(s + 16) = 180, di mana s adalah sisi persegi, maka pernyataan berikut yang benar adalah ...
= ...
Perhatikan gambar di atas. Gambar itu disebut …
Diketahui dua garis sejajar yang dipotong oleh sebuah garis lain. Pasangan sudut yang memiliki jumlah 180o adalah ....
Berikut ini yang tidak terdapat pada bagian identifikasi teks deskripsi adalah ….
Hasil dari
Cermati kutipan surat berikut ini.
Berdasarkan isi surat di atas, sifat si pengirim dulu waktu di sekolah adalah ....
Perhatikan penggalan buku fiksi berikut.
Hiruk pikuk bunyi kendaraan mulai memecahkan keheningan pagi. Jalan Veteran mulai ramai dipenuhi angkutan kota yang lalu-lalang. Ada yang pergi bekerja, ada yang hanya sekadar berjalan-jalan pagi. Ada yang ingin berangkat sekolah. Semuanya terlihat terburu-buru.
(Dikutip dari novel Origami Hati karya Boy Candra)
Unsur yang menonjol pada penggalan buku fiksi tersebut adalah ….
Kenaikan penjualan telur tertinggi terjadi pada bulan ....
Read the dialogue below and answer the question.
Pita : Hai, Marel. Can I ask you something? Marrel: Sure, what is it? Pita : Is your name spelled M-A-R-E-L? Marrel: No, It should be M-A-R-R-E-L.
Pita asks Marrel because she wants to know ....