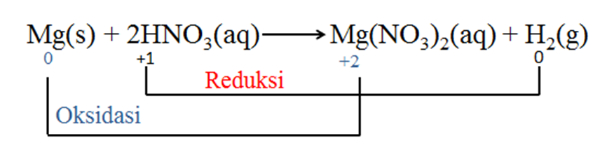
Bank Soal Kimia SMA Reaksi Redoks
Soal
LOTS
Soal Populer Hari Ini
Jenis sitoskeleton yang menyusun rambut manusia adalah ....
Biologi
Level 11
Biologi
Sel
Struktur dan Fungsi Sel
Jika setiap titik pada parabola ditranslasikan menurut 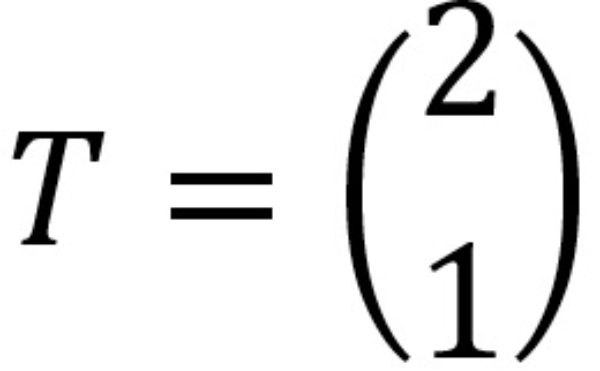 maka parabola yang dihasilkan adalah ....
maka parabola yang dihasilkan adalah ....
Matematika
Level 11
Geometri
Transformasi Geometri
Tranlasi
Complete the dialogue below.

Renny: I’ve been working since 8 in the morning. Now, I feel tired and hungry.
Dan: ______
Bahasa Inggris
Level 11
Good Advice
Giving Advice or Suggestions
Penamaan senyawa hidrokarbon alkuna berikut yang tidak sesuai dengan aturan adalah ....
Kimia
Level 11
Hidrokarbon dan Minyak Bumi
Hidrokarbon
Diketahui adalah rumus dari
Jika benar untuk , maka akan dibuktikan benar bahwa ....
Matematika
Level 11
Logika
Induksi Matematika
Induksi Matematika pada Barisan Bilangan
Perhatikan gambar berikut!

Sebuah benda berbentuk persegi panjang memiliki massa jenis yang tidak homogen. Massa jenis pada sisi merah lebih besar daripada massa jenis pada sisi biru. Letak titik berat benda tersebut yang mungkin adalah di posisi ....
Fisika
Level 11
Fisika
Dinamika dan Keseimbangan Benda Tegar
Titik Berat
Protein transpor berperan dalam transportasi zat seperti asam amino dan glukosa. Tidak adanya protein transpor ini bisa menyebabkan terjadinya suatu penyakit yang ditandai dengan terdapatnya sistein dalam jumlah besar pada air seni. Keberadaan sistein ini bisa menyebabkan terjadinya batu ginjal apabila asam amino itu terkristalisasi. Penyakit yang dimaksud dari pernyataan tersebut adalah ....
Biologi
Level 11
Biologi
Sel
Mekanisme Transpor Membran Plasma
Jenis reaksi yang terdapat pada persamaan reaksi berikut adalah ....
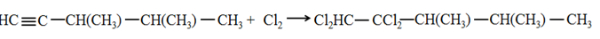
Kimia
Level 11
Hidrokarbon dan Minyak Bumi
Hidrokarbon
Himpunan penyelesaian untuk persamaan trigonometri pada interval adalah ....
Matematika
Level 11
Trigonometri
Persamaan Trigonometri
Berikut adalah daftar gelombang elektromagnetik yang terpapar oleh bumi.
- Gelombang radio
- Inframerah
- Cahaya tampak
- Ultraviolet
Gelombang elektromagnetik yang diserap oleh lapisan ozon adalah ....
Fisika
Level 11
Fisika
Pemanasan Global
Pemanasan Global dan Efek Rumah Kaca
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Jenis sitoskeleton yang menyusun rambut manusia adalah ....
Jika setiap titik pada parabola ditranslasikan menurut 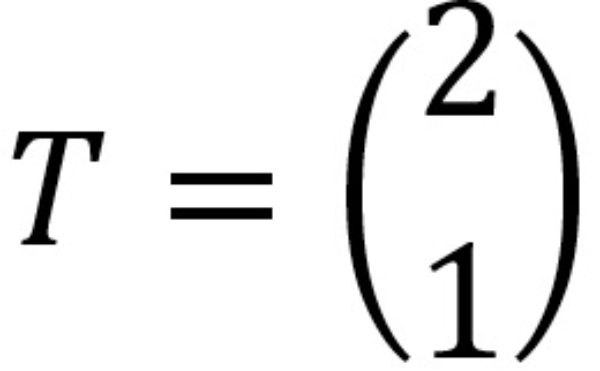
Complete the dialogue below.

Renny: I’ve been working since 8 in the morning. Now, I feel tired and hungry.
Dan: ______
Penamaan senyawa hidrokarbon alkuna berikut yang tidak sesuai dengan aturan adalah ....
Diketahui adalah rumus dari
Jika benar untuk , maka akan dibuktikan benar bahwa ....
Perhatikan gambar berikut!
Sebuah benda berbentuk persegi panjang memiliki massa jenis yang tidak homogen. Massa jenis pada sisi merah lebih besar daripada massa jenis pada sisi biru. Letak titik berat benda tersebut yang mungkin adalah di posisi ....
Protein transpor berperan dalam transportasi zat seperti asam amino dan glukosa. Tidak adanya protein transpor ini bisa menyebabkan terjadinya suatu penyakit yang ditandai dengan terdapatnya sistein dalam jumlah besar pada air seni. Keberadaan sistein ini bisa menyebabkan terjadinya batu ginjal apabila asam amino itu terkristalisasi. Penyakit yang dimaksud dari pernyataan tersebut adalah ....
Jenis reaksi yang terdapat pada persamaan reaksi berikut adalah ....
Himpunan penyelesaian untuk persamaan trigonometri pada interval adalah ....
Berikut adalah daftar gelombang elektromagnetik yang terpapar oleh bumi.
- Gelombang radio
- Inframerah
- Cahaya tampak
- Ultraviolet
Gelombang elektromagnetik yang diserap oleh lapisan ozon adalah ....