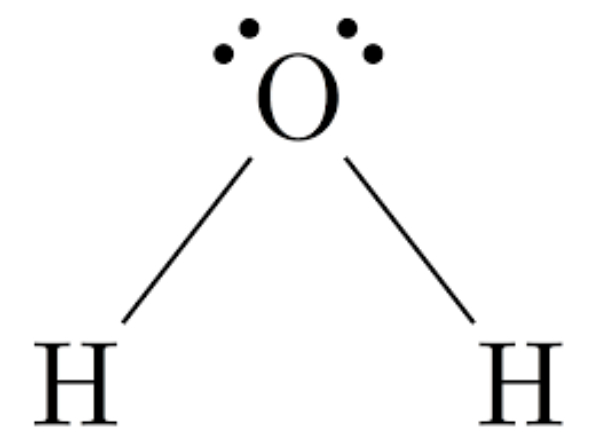
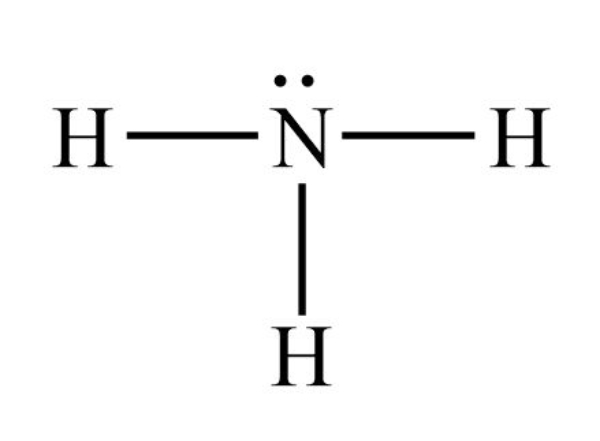
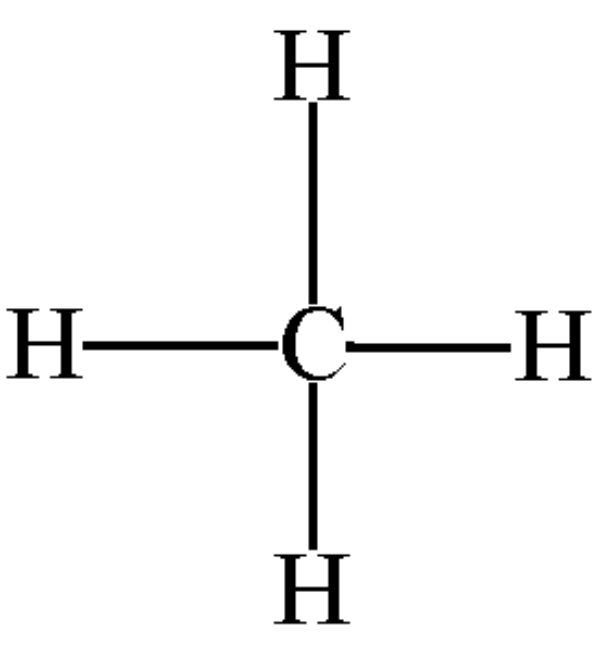
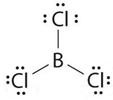
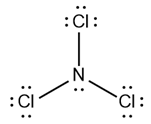
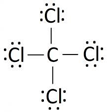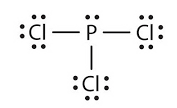Bank Soal Kimia SMA Ikatan Hidrogen dan Gaya van der Waals
Soal
LOTS Memahami
Soal Populer Hari Ini
Perhatikan garis bilangan dibawah ini!
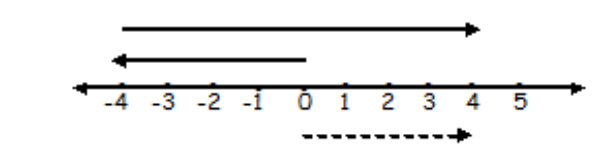
Kalimat matematika yang sesuai dengan gambar di atas adalah ...
Matematika
Level 6
Bilangan
Operasi Hitung Bilangan Bulat dan Pecahan
Operasi Hitung Bilangan Bulat
Pay attention to the following picture.

Which vehicle travels in this place?
Bahasa Inggris
Level 6
Bahasa Inggris
Past Holidays
Vocabulary: Places for Holidays and Vehicles
Perhatikan penggalan paragraf dalam buku sejarah berikut!

(Sumber gambar: kebudayaan.kemdikbud.go.id)
Pada tahun 1900, di saat bangsa Indonesia mulai terbuka dalam berpikir, cara perjuangan untuk merebut kemerdekaan juga mulai menggunakan pendekatan organisasi pergerakan. Hal itu didukung juga oleh pengubahan kebijakan dari penjajah Belanda dengan mengizinkan berdirinya sekolah peribumi. Sejarah mencatat beberapa organisasi pergerakan kemerdekaan yang memengaruhi perjalanan bangsa Indonesia sampai dengan tercapainya kemerdekaan Indonesia. Adapun organisasi pergerakan tersebut antara lain adalah Budi Utomo, Sarekat Islam, Muhammadiyah, Gerakan Pemuda,Taman Siswa, Gerakan Wanita, Partai Nasional Indonesia (PNI), dan Gerakan Buruh.
Agar kalimat yang bercetak tebal menjadi kalimat efektif maka kata yang harus diubah adalah ....
Bahasa Indonesia
Level 6
Membaca
Buku Sejarah
Mengembangkan Informasi
Sebuah kerucut mempunyai jari-jari alas 14 cm dan tinggi 15 cm. Volume kerucut tersebut adalah ... cm3.
Matematika
Level 6
Geometri
Bangun Ruang
Volume dan Luas Permukaan Bangun Ruang
Hasil
Matematika
Level 6
Bilangan
Operasi Hitung Bilangan Bulat dan Pecahan
Operasi Hitung Bilangan Bulat

Ibu membeli sebuah caping dari pasar. Caping tersebut berbentuk kerucut tanpa alas seperti gambar di atas. Luas permukaan caping tersebut adalah ... cm2 ( Gunakan = 3,14 )
Matematika
Level 6
Geometri
Bangun Ruang
Volume dan Luas Permukaan Bangun Ruang
Bacalah laporan berikut!
Pada tanggal 12 Juni 2019 pagi hari, siswa kelas IV melakukan pengamatan di Pasar Hewan Dimoro. Banyak jenis sapi didatangkan dari peternakan di Malang, Ponorogo, hingga Probolinggo oleh para pedagang. Berbagai jenis sapi, seperti sapi limosin, sapi brahman, hingga sapi lokal ada di sana. [...]
Kalimat simpulan yang tepat untuk melengkapi teks laporan hasil pengamatan di atas agar menjadi laporan yang padu adalah ...
Bahasa Indonesia
Level 6
Menulis
Teks Laporan Hasil Pengamatan
Menulis Teks Laporan
Sumber makanan terbaik yang harus dikonsumsi bayi saat baru lahir adalah ….
IPA
Level 6
Biologi
Perkembangbiakan Makhluk Hidup
Perkembangbiakan Manusia
Jika nilai a = , b = dan c = , maka hasil dari adalah ...
Saya ucapkan terima kasih karena telah memberikan kesempatan kepada saya untuk berpidato pada kesempatan kali ini. Pada kesempatan kali ini, saya akan menyampaikan pentingnya menjaga kebersihan kelas.
Penggalan teks pidato tersebut merupakan bagian ….
Bahasa Indonesia
Level 6
Membaca
Teks Pidato
Menggali Isi
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Perhatikan garis bilangan dibawah ini!
Kalimat matematika yang sesuai dengan gambar di atas adalah ...
Pay attention to the following picture.

Which vehicle travels in this place?
Perhatikan penggalan paragraf dalam buku sejarah berikut!
(Sumber gambar: kebudayaan.kemdikbud.go.id)
Pada tahun 1900, di saat bangsa Indonesia mulai terbuka dalam berpikir, cara perjuangan untuk merebut kemerdekaan juga mulai menggunakan pendekatan organisasi pergerakan. Hal itu didukung juga oleh pengubahan kebijakan dari penjajah Belanda dengan mengizinkan berdirinya sekolah peribumi. Sejarah mencatat beberapa organisasi pergerakan kemerdekaan yang memengaruhi perjalanan bangsa Indonesia sampai dengan tercapainya kemerdekaan Indonesia. Adapun organisasi pergerakan tersebut antara lain adalah Budi Utomo, Sarekat Islam, Muhammadiyah, Gerakan Pemuda,Taman Siswa, Gerakan Wanita, Partai Nasional Indonesia (PNI), dan Gerakan Buruh.
Agar kalimat yang bercetak tebal menjadi kalimat efektif maka kata yang harus diubah adalah ....
Sebuah kerucut mempunyai jari-jari alas 14 cm dan tinggi 15 cm. Volume kerucut tersebut adalah ... cm3.
Hasil
Ibu membeli sebuah caping dari pasar. Caping tersebut berbentuk kerucut tanpa alas seperti gambar di atas. Luas permukaan caping tersebut adalah ... cm2 ( Gunakan = 3,14 )
Bacalah laporan berikut!
Pada tanggal 12 Juni 2019 pagi hari, siswa kelas IV melakukan pengamatan di Pasar Hewan Dimoro. Banyak jenis sapi didatangkan dari peternakan di Malang, Ponorogo, hingga Probolinggo oleh para pedagang. Berbagai jenis sapi, seperti sapi limosin, sapi brahman, hingga sapi lokal ada di sana. [...]
Kalimat simpulan yang tepat untuk melengkapi teks laporan hasil pengamatan di atas agar menjadi laporan yang padu adalah ...
Sumber makanan terbaik yang harus dikonsumsi bayi saat baru lahir adalah ….
Jika nilai a = , b = dan c = , maka hasil dari adalah ...
Saya ucapkan terima kasih karena telah memberikan kesempatan kepada saya untuk berpidato pada kesempatan kali ini. Pada kesempatan kali ini, saya akan menyampaikan pentingnya menjaga kebersihan kelas.
Penggalan teks pidato tersebut merupakan bagian ….