Bank Soal Kimia SMA Halogen
Soal
Soal Populer Hari Ini
Kelompok lipid yang terlibat dalam penyusun lapisan kutikula pada permukaan daun tanaman adalah ....
Biologi
Level 11
Biologi
Sel
Penemuan, Tipe, Ukuran, dan Komponen Kimiawi Sel
Jika titik ditranslasikan oleh 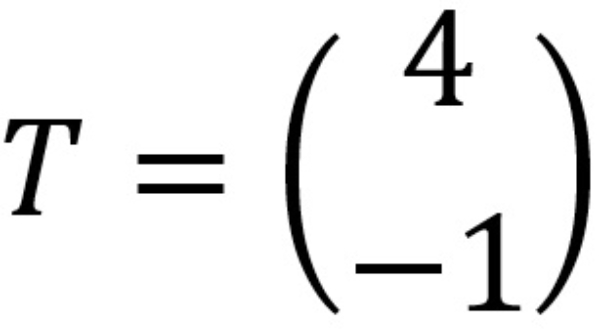 maka bayangan titik adalah ....
maka bayangan titik adalah ....
Matematika
Level 11
Geometri
Transformasi Geometri
Tranlasi
Choose the right offer for the following situation.

You look at your friend in front of his apartment. He can’t move the heavy boxes.
Bahasa Inggris
Level 11
Good Advice
Making Offers
Reaksi berikut yang tidak bisa terjadi pada senyawa hidrokarbon alkuna adalah ....
Kimia
Level 11
Hidrokarbon dan Minyak Bumi
Hidrokarbon
Diketahui . Nilai dari
Matematika
Level 11
Logika
Induksi Matematika
Notasi Sigma
Pernyataan yang benar tentang momen inersia adalah ....
Fisika
Level 11
Fisika
Dinamika dan Keseimbangan Benda Tegar
Dinamika Benda Tegar
Perhatikan struktur di bawah ini!
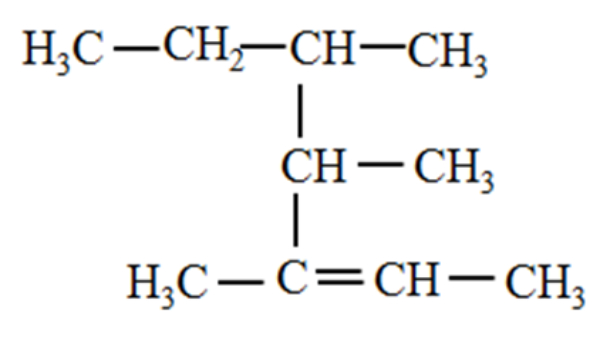
Tata nama dari struktur tersebut adalah ....
Kimia
Level 11
Hidrokarbon dan Minyak Bumi
Hidrokarbon
Di bawah ini molekul yang paling mudah memasuki sel adalah ....
Biologi
Level 11
Biologi
Sel
Mekanisme Transpor Membran Plasma
Himpunan penyelesaian dari persamaan trigonometri dengan adalah ....
Matematika
Level 11
Trigonometri
Persamaan Trigonometri
Perhatikan tabel emisi karbon dioksida dalam setahun dari negara-negara berikut!

Negara mana yang memiliki emisi per kapita terkecil?
Fisika
Level 11
Fisika
Pemanasan Global
Pemanasan Global dan Efek Rumah Kaca
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Kelompok lipid yang terlibat dalam penyusun lapisan kutikula pada permukaan daun tanaman adalah ....
Jika titik ditranslasikan oleh 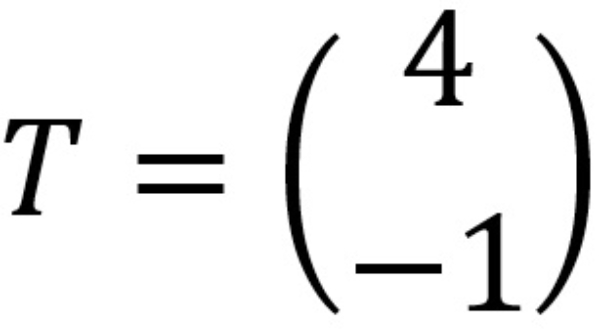
Choose the right offer for the following situation.

You look at your friend in front of his apartment. He can’t move the heavy boxes.
Reaksi berikut yang tidak bisa terjadi pada senyawa hidrokarbon alkuna adalah ....
Diketahui . Nilai dari
Pernyataan yang benar tentang momen inersia adalah ....
Perhatikan struktur di bawah ini!
Tata nama dari struktur tersebut adalah ....
Di bawah ini molekul yang paling mudah memasuki sel adalah ....
Himpunan penyelesaian dari persamaan trigonometri dengan adalah ....
Perhatikan tabel emisi karbon dioksida dalam setahun dari negara-negara berikut!
Negara mana yang memiliki emisi per kapita terkecil?







