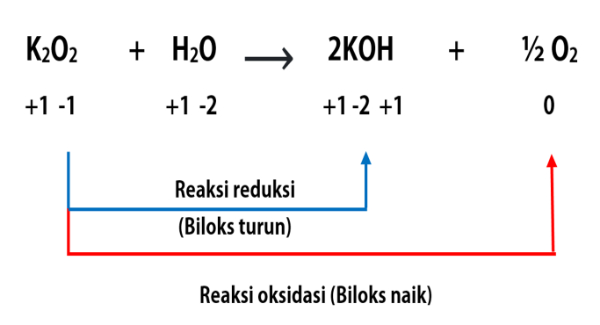
Bank Soal Kimia SMA Logam Alkali
Soal
Soal Populer Hari Ini
sama dengan ...
Pilih semua jawaban yang benar.
Matematika
Level 4
Bilangan
Pecahan
Bentuk Pecahan

Bangun pada gambar memiliki simetri putar sebanyak …
Matematika
Level 6
Geometri
Bangun Datar
Di bawah ini adalah macam-macam karya sastra, kecuali ....
Bahasa Indonesia
Level 4
Membaca
Buku Sastra
Ulasan Buku Sastra
Fill the blanks with 'a' or 'an'.
1. I want to be ... surgeon.
2. She is ... architect.
The correct answers for number 1 and 2 are ....
Bahasa Inggris
Level 4
Bahasa Inggris
Jobs
Vocabulary: Jobs
Faktor persekutuan dari 32 dan 36 adalah …
Matematika
Level 4
Bilangan
Faktor dan Kelipatan
Faktor Persekutuan
Poligon yang mempunyai 7 sisi dinamakan?
Matematika
Level 4
Geometri
Bangun Datar
Segi Banyak
Faktorisasi prima dari 48 adalah …
Matematika
Level 4
Bilangan
FPB dan KPK
Faktor dan Faktorisasi Prima
Legenda Kanjeng Ratu Kidul (Jawa)

Suatu malam Pangeran Panembahan Senopati bertapa di Pantai Parang Kusumo. Dengan bertapa, ia bermaksud ingin menemukan cara untuk menaklukkan Kesultanan Pajang. Jika Kesultanan Pajang berhasil ditaklukkan, maka ia ingin membangun kerajaan baru yang dinamakan Mataram.
Tapanya sangat khusyuk hingga terjadi gelombang dahsyat yang mengganggu Laut Selatan. Penguasa Laut Selatan, Kanjeng Ratu Kidul, segera datang memeriksa ke pantai. Begitu melihat Panembahan Senopati yang gagah dan tampan sedang bertapa, sang Ratu seketika jatuh cinta. Sang Ratu meminta Panembahan Senopati untuk menikah dengannya.
Panembahan Senopati menyanggupi permintaan Kanjeng Ratu Kidul. Sang Ratu pun mengerahkan lelembut Laut Selatan untuk membantu sang Pangeran menaklukkan Kesultanan Pajang. Serangan mereka berhasil! Kesultanan Pajang kalah dan Kesultanan Mataram didirikan. Sang Ratu pun menjadi pasangan spiritual sang Pangeran. Tidak hanya itu, sang Ratu juga menjadi pasangan spiritual bagi semua raja Mataram yang akan datang.
(Sumber: dongengceritarakyat.com, wikipedia)
Tokoh yang dikalahkan Panembahan Senopati dalam cerita di atas adalah ....
Bahasa Indonesia
Level 4
Membaca
Teks Fiksi-Tokoh Cerita
Cerita Rakyat
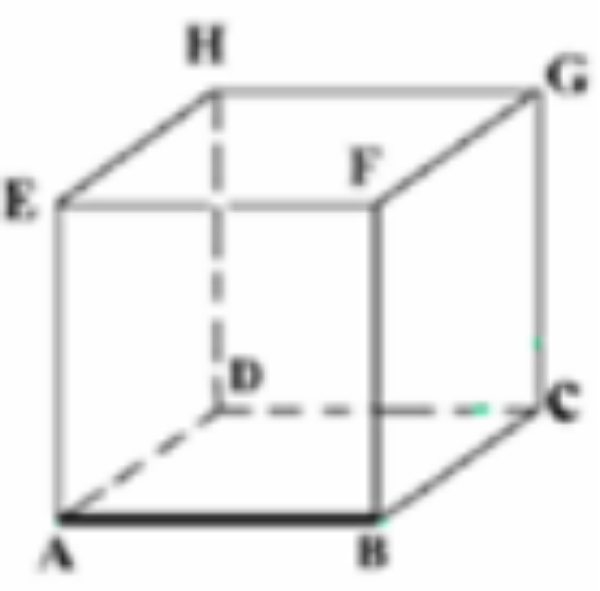
Berdasarkan kubus ABCD.EFGH, bidang yang berpotongan adalah ...
Matematika
Level 4
Geometri
Garis dan Sudut
Hubungan Antar Garis
Berikut adalah diagram batang nama makanan dan jumlah porsi yang berhasil terjual hari ini di rumah makan Bu Tuni.
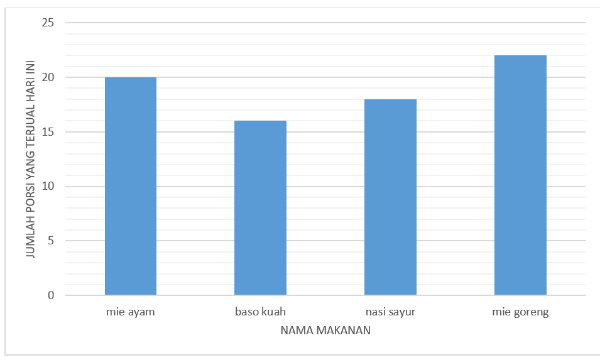
Berapa porsi bakso kuah yang terjual?
Matematika
Level 4
Statistika
Bentuk Diagram
Membaca Diagram
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
sama dengan ...
Pilih semua jawaban yang benar.
Bangun pada gambar memiliki simetri putar sebanyak …
Di bawah ini adalah macam-macam karya sastra, kecuali ....
Fill the blanks with 'a' or 'an'.
1. I want to be ... surgeon.
2. She is ... architect.
The correct answers for number 1 and 2 are ....
Faktor persekutuan dari 32 dan 36 adalah …
Poligon yang mempunyai 7 sisi dinamakan?
Faktorisasi prima dari 48 adalah …
Legenda Kanjeng Ratu Kidul (Jawa)
Suatu malam Pangeran Panembahan Senopati bertapa di Pantai Parang Kusumo. Dengan bertapa, ia bermaksud ingin menemukan cara untuk menaklukkan Kesultanan Pajang. Jika Kesultanan Pajang berhasil ditaklukkan, maka ia ingin membangun kerajaan baru yang dinamakan Mataram.
Tapanya sangat khusyuk hingga terjadi gelombang dahsyat yang mengganggu Laut Selatan. Penguasa Laut Selatan, Kanjeng Ratu Kidul, segera datang memeriksa ke pantai. Begitu melihat Panembahan Senopati yang gagah dan tampan sedang bertapa, sang Ratu seketika jatuh cinta. Sang Ratu meminta Panembahan Senopati untuk menikah dengannya.
Panembahan Senopati menyanggupi permintaan Kanjeng Ratu Kidul. Sang Ratu pun mengerahkan lelembut Laut Selatan untuk membantu sang Pangeran menaklukkan Kesultanan Pajang. Serangan mereka berhasil! Kesultanan Pajang kalah dan Kesultanan Mataram didirikan. Sang Ratu pun menjadi pasangan spiritual sang Pangeran. Tidak hanya itu, sang Ratu juga menjadi pasangan spiritual bagi semua raja Mataram yang akan datang.
(Sumber: dongengceritarakyat.com, wikipedia)
Tokoh yang dikalahkan Panembahan Senopati dalam cerita di atas adalah ....
Berdasarkan kubus ABCD.EFGH, bidang yang berpotongan adalah ...
Berikut adalah diagram batang nama makanan dan jumlah porsi yang berhasil terjual hari ini di rumah makan Bu Tuni.
Berapa porsi bakso kuah yang terjual?