Bank Soal Kimia SMA Hukum, Tetapan, dan Pergeseran Kesetimbangan
Soal
LOTS Memahami
Soal Populer Hari Ini
Budi memiliki sebuah bambu sepanjang m. Karena terlalu panjang, bambu itu dipotong dan dibuang m . Panjang bambu itu sekarang adalah ...
Matematika
Level 5
Bilangan
Operasi Hitung Pecahan
Operasi Hitung Pecahan Biasa dan Campuran
Wilayah di Indonesia yang menggunakan sungai sebagai tempat untuk melakukan perdagangan adalah ....
IPS
Level 5
Geografi
Karakteristik Geografi Wilayah Indonesia
Pengaruh Kondisi Geografis terhadap Kehidupan
Mendorong, membujuk, atau memberikan pengaruh pada banyak orang agar tertarik pada barang atau jasa yang ditawarkan merupakan fungsi dari ....
Bahasa Indonesia
Level 5
Membaca
Iklan
Identifikasi Informasi
Read the following table.

Template source: canva.com
Which sentence is best to complete the table?
Bahasa Inggris
Level 5
Bahasa Inggris
Friendship
Greeting & Leave Taking
Sebuah bak mandi terisi air sebanyak 1.500 liter. Agar bak tersebut dapat terisi 2 m3 air, maka volume bak harus ditambah sebanyak … m3.
Matematika
Level 5
Geometri
Perbandingan Dua Besaran
Debit
Perhatikan gambar berikut!
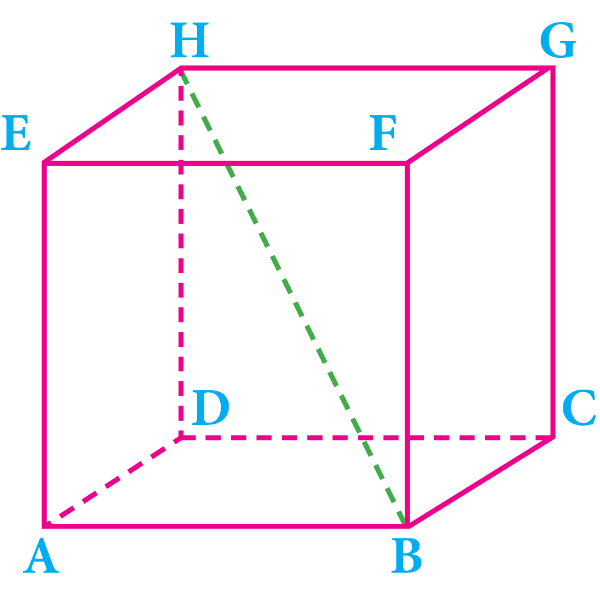
Garis hijau yang menghubungkan titik B dengan tittik H pada gambar kubus di atas disebut ....
Matematika
Level 5
Geometri
Balok dan Kubus
Sifat dan Jaring-Jaring Balok dan Kubus
Wayan dan Mirna berjualan kopi selama 4 hari yaitu Senin, Selasa, Rabu, Kamis. Jika minimal penjualan dalam sehari adalah 150 dan hasil penjualan tidak pernah lebih dari hari sebelumnya, maka manakah tabel dibawah yang tepat?
Matematika
Level 5
Statistika
Pengumpulan dan Penyajian Data
Menyajikan Data
Berikut adalah diagram yang menunjukkan alat transportasi yang digunakan siswa untuk ke sekolah.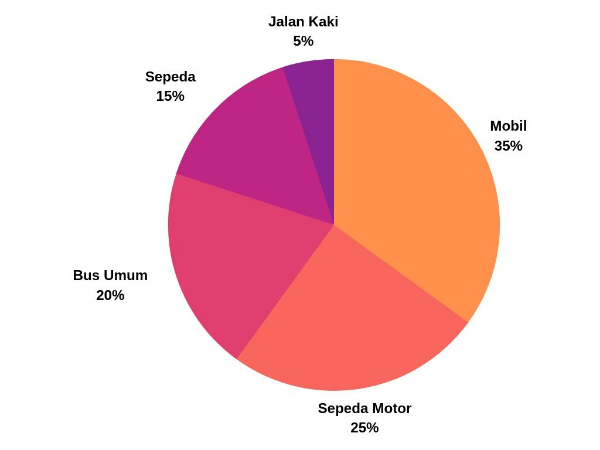
Jika 16 siswa menggunakan bus umum untuk berangkat sekolah, maka siswa yang menggunakan sepeda saat berangkat sekolah sebanyak ... siswa
Matematika
Level 5
Statistika
Pengumpulan dan Penyajian Data
Membaca Data
Bacalah teks berikut!
Adat istiadat merupakan suatu sistem norma atau tata kelakuan yang tumbuh, berkembang, dan dijunjung tinggi oleh masyarakat secara turun-temurun. Adat istiadat juga merupakan kebiasaan sosial yang sejak lama telah ada di masyarakat dan bertujuan untuk mengatur tata tertib dalam masyarakat tersebut.
Keberagaman budaya menjadikan adat istiadat beragam pula. Adat istiadat terbentuk sesuai dengan kebiasaan masyarakat setempat. Setiap suku yang ada di Indonesia memiliki adat istiadat yang berbeda. Sebagai contoh, tradisi masyarakat Jawa berbeda dengan masyarakat NTT, Bali, maupun Papua. Adat istiadat memiliki aturan khusus yang mengikat masyarakat. Adat istiadat memiliki nilai budaya yang luhur, bersifat mengikat suatu kelompok masyarakat yang tinggal di daerah tertentu, dan memiliki sistem hukum yang tegas bagi seluruh masyarakat.
Meskipun setiap daerah memiliki adat istiadatnya masing-masing, namun Indonesia harus tetap hidup rukun dan damai. Saling menghormati antar suku dan budaya seperti semboyan Bangsa Indonesia yaitu Bhinneka Tunggal Ika, yang artinya berbeda-beda tetapi tetap satu. Perbedaan juga menjadi sebuah kekuatan sehingga memperkaya sifat budaya bangsa Indonesia serta persatuan dan kesatuan bangsa.
Teks tersebut termasuk jenis eksplanasi ....
Bahasa Indonesia
Level 5
Membaca
Teks Eksplanasi
Informasi Penting dalam Teks
Cermati contoh surat berikut ini.

Tujuan Dinas Kebudayaan Kota Cirebon mengadakan lomba Melukis dari Rumah adalah ....
Bahasa Indonesia
Level 5
Membaca
Surat Undangan
Identifikasi Surat Undangan
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Budi memiliki sebuah bambu sepanjang m. Karena terlalu panjang, bambu itu dipotong dan dibuang m . Panjang bambu itu sekarang adalah ...
Wilayah di Indonesia yang menggunakan sungai sebagai tempat untuk melakukan perdagangan adalah ....
Mendorong, membujuk, atau memberikan pengaruh pada banyak orang agar tertarik pada barang atau jasa yang ditawarkan merupakan fungsi dari ....
Read the following table.
Template source: canva.com
Which sentence is best to complete the table?
Sebuah bak mandi terisi air sebanyak 1.500 liter. Agar bak tersebut dapat terisi 2 m3 air, maka volume bak harus ditambah sebanyak … m3.
Perhatikan gambar berikut!
Garis hijau yang menghubungkan titik B dengan tittik H pada gambar kubus di atas disebut ....
Wayan dan Mirna berjualan kopi selama 4 hari yaitu Senin, Selasa, Rabu, Kamis. Jika minimal penjualan dalam sehari adalah 150 dan hasil penjualan tidak pernah lebih dari hari sebelumnya, maka manakah tabel dibawah yang tepat?
Berikut adalah diagram yang menunjukkan alat transportasi yang digunakan siswa untuk ke sekolah.
Jika 16 siswa menggunakan bus umum untuk berangkat sekolah, maka siswa yang menggunakan sepeda saat berangkat sekolah sebanyak ... siswa
Bacalah teks berikut!
Adat istiadat merupakan suatu sistem norma atau tata kelakuan yang tumbuh, berkembang, dan dijunjung tinggi oleh masyarakat secara turun-temurun. Adat istiadat juga merupakan kebiasaan sosial yang sejak lama telah ada di masyarakat dan bertujuan untuk mengatur tata tertib dalam masyarakat tersebut.
Keberagaman budaya menjadikan adat istiadat beragam pula. Adat istiadat terbentuk sesuai dengan kebiasaan masyarakat setempat. Setiap suku yang ada di Indonesia memiliki adat istiadat yang berbeda. Sebagai contoh, tradisi masyarakat Jawa berbeda dengan masyarakat NTT, Bali, maupun Papua. Adat istiadat memiliki aturan khusus yang mengikat masyarakat. Adat istiadat memiliki nilai budaya yang luhur, bersifat mengikat suatu kelompok masyarakat yang tinggal di daerah tertentu, dan memiliki sistem hukum yang tegas bagi seluruh masyarakat.
Meskipun setiap daerah memiliki adat istiadatnya masing-masing, namun Indonesia harus tetap hidup rukun dan damai. Saling menghormati antar suku dan budaya seperti semboyan Bangsa Indonesia yaitu Bhinneka Tunggal Ika, yang artinya berbeda-beda tetapi tetap satu. Perbedaan juga menjadi sebuah kekuatan sehingga memperkaya sifat budaya bangsa Indonesia serta persatuan dan kesatuan bangsa.
Teks tersebut termasuk jenis eksplanasi ....
Cermati contoh surat berikut ini.
Tujuan Dinas Kebudayaan Kota Cirebon mengadakan lomba Melukis dari Rumah adalah ....