Bank Soal Kimia SMA Kenaikan Titik Didih Larutan
Soal
Soal Populer Hari Ini
Sebuah toko bunga menerima pesanan karangan bunga setiap hari.
Karangan bunga yang dibuat membutuhkan banyak bunga mawar.
Setiap satu rangkaian bunga besar membutuhkan 326 tangkai mawar.
Banyak mawar digambarkan sebagai berikut.
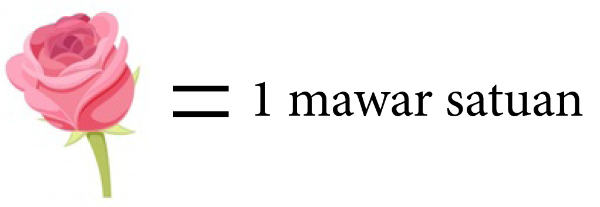
Mawar yang berjumlah sepuluh tangkai digambarkan menjadi 1 mawar puluhan.
Dan mawar puluhan yang berjumlah sepuluh digambarkan menjadi mawar ratusan.
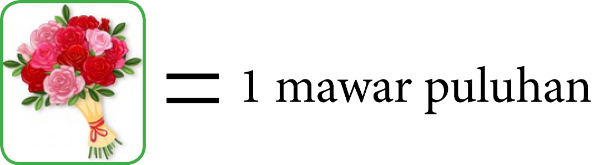
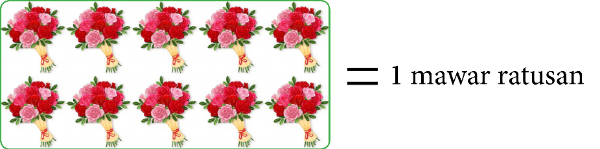
Banyak bunga mawar yang sesuai untuk membuat satu karangan bunga besar ditunjukkan oleh gambar ....
Matematika
Level 2
Bilangan
Mengenal Bilangan Cacah (0-999)
Mengenal Bilangan Sampai 999
Ayo, kita membersihkan rumah bersama.
Gambar yang sesuai dengan ungkapan perintah di atas adalah ....
Bahasa Indonesia
Level 2
Menulis
Ungkapan (1)
Ungkapan Ajakan
Asa pergi ke toko.
Di toko tersebut menjual berbagai macam alat tulis.
Berikut adalah daftar harga berbagai macam alat tulis yang dijual.

(Sumber Gambar: flaticon.com)
Asa memiliki 1 lembar uang dua ribuan.
Ia ingin menggunakan uangnya untuk membeli 2 jenis barang tetapi masih mendapatkan uang kembalian.
Barang yang dapat dibeli Asa adalah ....
Matematika
Level 2
Bilangan
Nilai dan Kesetaraan Mata Uang
Kesetaraan Nilai Mata Uang
Gambar yang tepat untuk melanjutkan pola barisan berikut ini adalah ....

(Sumber: freepik.com)
Matematika
Level 2
Geometri
Bangun Ruang sederhana
Pola Barisan Bangun Ruang
Bu Ina ingin membeli kain batik.
Pilihan motif kain yang tersedia adalah sebagai berikut.

(Sumber Gambar: freepik.com)
Bu Ina memilih model kain batik dengan motif menyerupai bangun datar persegi panjang.
Motif kain batik yang dipilih Bu Ina adalah ....
Matematika
Level 2
Geometri
Bangun Datar Sederhana
Ciri-Ciri Bangun Datar Sederhana
Perhatikan gambar berikut!


(Sumber Gambar: id.wikipedia.org)
Pecahan uang yang setara dengan uang pada gambar di atas adalah ....
Matematika
Level 2
Bilangan
Nilai dan Kesetaraan Mata Uang
Kesetaraan Nilai Mata Uang
Arrange the jumbled letters.

Source: canva
Bahasa Inggris
Level 2
A NEW FRIEND
Shape and Colour
Jam yang menunjukkan pukul 5.00 adalah ....
Matematika
Level 2
Bilangan
Satuan Waktu, Panjang, dan Berat
Mengenal Alat Ukur Waktu
Terdapat dua buah bilangan.
Kedua bilangan memiliki nilai ratusan yang sama.
Tetapi bilangan pertama memiliki nilai puluhan yang lebih besar dari bilangan kedua.
Sebaliknya, nilai satuan pada bilangan kedua lebih besar dari bilangan pertama.
Bilangan pertama dan kedua berturut-turut yang sesuai adalah ....
Matematika
Level 2
Bilangan
Mengenal Bilangan Cacah (0-999)
Menentukan Nilai Tempat Bilangan
Ayah membeli martabak manis hari ini.

Budi mendapatkan 1 potong martabak manis.
Banyak potongan martabak yang didapat oleh Budi dalam bentuk pecahan adalah ....
Matematika
Level 2
Bilangan
Konsep Pecahan
Konsep Pecahan
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Sebuah toko bunga menerima pesanan karangan bunga setiap hari.
Karangan bunga yang dibuat membutuhkan banyak bunga mawar.
Setiap satu rangkaian bunga besar membutuhkan 326 tangkai mawar.
Banyak mawar digambarkan sebagai berikut.
Mawar yang berjumlah sepuluh tangkai digambarkan menjadi 1 mawar puluhan.
Dan mawar puluhan yang berjumlah sepuluh digambarkan menjadi mawar ratusan.
Banyak bunga mawar yang sesuai untuk membuat satu karangan bunga besar ditunjukkan oleh gambar ....
Ayo, kita membersihkan rumah bersama.
Gambar yang sesuai dengan ungkapan perintah di atas adalah ....
Asa pergi ke toko.
Di toko tersebut menjual berbagai macam alat tulis.
Berikut adalah daftar harga berbagai macam alat tulis yang dijual.
(Sumber Gambar: flaticon.com)
Asa memiliki 1 lembar uang dua ribuan.
Ia ingin menggunakan uangnya untuk membeli 2 jenis barang tetapi masih mendapatkan uang kembalian.
Barang yang dapat dibeli Asa adalah ....
Gambar yang tepat untuk melanjutkan pola barisan berikut ini adalah ....
(Sumber: freepik.com)
Bu Ina ingin membeli kain batik.
Pilihan motif kain yang tersedia adalah sebagai berikut.
(Sumber Gambar: freepik.com)
Bu Ina memilih model kain batik dengan motif menyerupai bangun datar persegi panjang.
Motif kain batik yang dipilih Bu Ina adalah ....
Perhatikan gambar berikut!
(Sumber Gambar: id.wikipedia.org)
Pecahan uang yang setara dengan uang pada gambar di atas adalah ....
Arrange the jumbled letters.
Source: canva
Jam yang menunjukkan pukul 5.00 adalah ....
Terdapat dua buah bilangan.
Kedua bilangan memiliki nilai ratusan yang sama.
Tetapi bilangan pertama memiliki nilai puluhan yang lebih besar dari bilangan kedua.
Sebaliknya, nilai satuan pada bilangan kedua lebih besar dari bilangan pertama.
Bilangan pertama dan kedua berturut-turut yang sesuai adalah ....
Ayah membeli martabak manis hari ini.
Budi mendapatkan 1 potong martabak manis.
Banyak potongan martabak yang didapat oleh Budi dalam bentuk pecahan adalah ....







