Bank Soal Kimia SMA Konsep Kelarutan dan Hasil Kali Kelarutan
Soal
Soal Populer Hari Ini
Dua buah uang logam dilempar secara bersama-sama sebanyak 48 kali. Berapa frekuensi harapan muncul 2 gambar?
Matematika
Level 8
Statistika
Peluang
Frekuensi Harapan
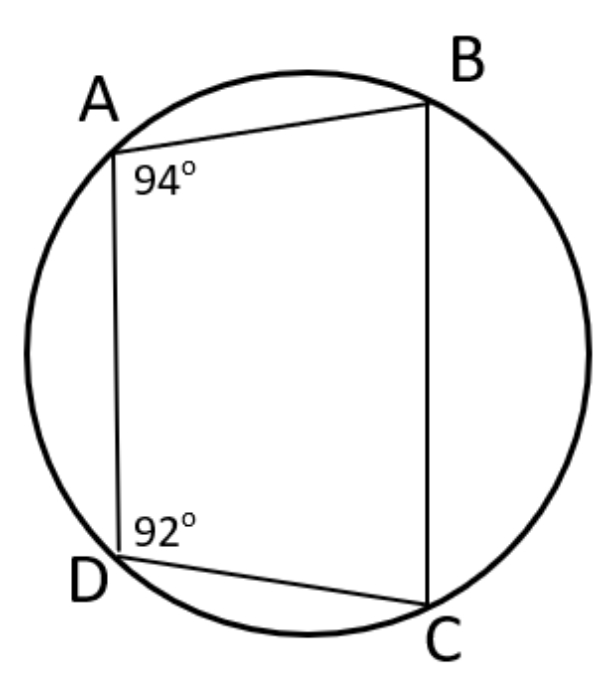
Jika dan , maka perbandingan terhadap adalah ...
Matematika
Level 8
Geometri
Lingkaran
Luas dan Keliling Lingkaran
Perhatikan gambar berikut!
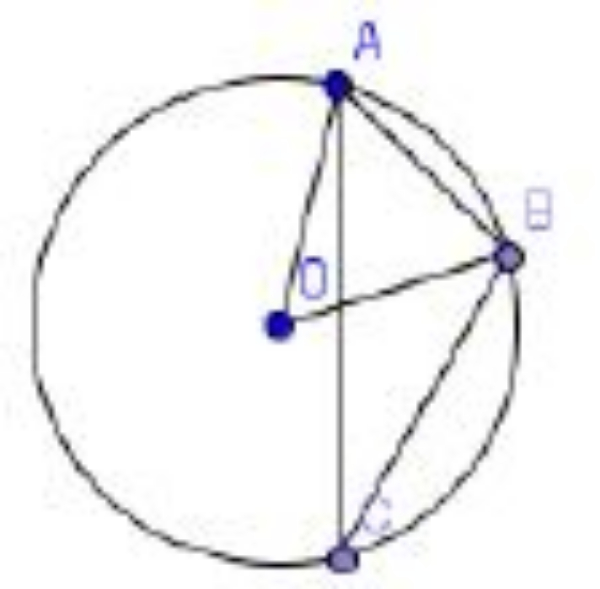
Jika sudut ABO = 55o, hitunglah besar sudut ACB!
Matematika
Level 8
Geometri
Lingkaran
Suatu segitiga siku-siku PQR mempunyai luas 15 satuan luas. Jika titik P(-2, 6) dan R(-2, 1) sedangkan Q di kuadran I, maka koordinat titik Q yang mungkin adalah?
Matematika
Level 8
Geometri
Koordinat Kartesius
Pengertian berita adalah ....
Bahasa Indonesia
Level 8
Menulis
Teks Berita
Unsur-unsur Berita
Kinan — drive — patient — all my friends.
The correct superlative adverb based on the clues is ...
Bahasa Inggris
Level 8
Bahasa Inggris
Comparisons of people or things
Degrees of Comparison of Adverbs
Di antara titik berikut, manakah yang memiliki tempat kedudukan paling kiri?
Matematika
Level 8
Geometri
Koordinat Kartesius
Posisi Titik dan Bangun Datar
Bacalah puisi berikut ini!
Diponegoro
Di masa pembangunan ini
Tuan hidup kembali
Dan bara kagum menjadi api
Di depan sekali tuan menanti
Tak gentar. Lawan banyaknya seratus kali.
Pedang di kanan, keris di kiri
Berselempang semangat yang tak bisa mati.
MAJU
Ini barisan tak bergenderang-berpalu
Kepercayaan tanda menyerbu.
Sekali berarti
Sudah itu mati.
MAJU
Bagimu negeri
Menyediakan api.
Punah di atas menghamba
Binasa di atas ditindas
Sungguhpun dalam ajal baru tercapai
Jika hidup harus merasai
Maju.
Serbu.
Serang.
Terjang.
(Diadaptasi dari buku "Aku Ini Binatang Jalang" karya Chairil Anwar)
Struktur lahir yang menonjol dari puisi tersebut adalah ....
Bahasa Indonesia
Level 8
Menulis
Puisi
Unsur-unsur puisi
Berikut ini yang tidak termasuk bagian-bagian iklan, yaitu ....
Bahasa Indonesia
Level 8
Menulis
Iklan, Slogan, Poster
Unsur-unsur Iklan, Slogan, Poster
Look at the following picture.

Source: wisdomquotesandstories.com
What will you do if you see this?
Bahasa Inggris
Level 8
Bahasa Inggris
Interaction among students inside and outside classrooms
Expressions of Willingness to Do Something
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Dua buah uang logam dilempar secara bersama-sama sebanyak 48 kali. Berapa frekuensi harapan muncul 2 gambar?
Jika dan , maka perbandingan terhadap adalah ...
Perhatikan gambar berikut!
Jika sudut ABO = 55o, hitunglah besar sudut ACB!
Suatu segitiga siku-siku PQR mempunyai luas 15 satuan luas. Jika titik P(-2, 6) dan R(-2, 1) sedangkan Q di kuadran I, maka koordinat titik Q yang mungkin adalah?
Pengertian berita adalah ....
Kinan — drive — patient — all my friends.
The correct superlative adverb based on the clues is ...
Di antara titik berikut, manakah yang memiliki tempat kedudukan paling kiri?
Bacalah puisi berikut ini!
Diponegoro
Di masa pembangunan ini Tuan hidup kembali Dan bara kagum menjadi api Di depan sekali tuan menanti Tak gentar. Lawan banyaknya seratus kali. Pedang di kanan, keris di kiri Berselempang semangat yang tak bisa mati. MAJU Ini barisan tak bergenderang-berpalu Kepercayaan tanda menyerbu. Sekali berarti Sudah itu mati. MAJU Bagimu negeri Menyediakan api. Punah di atas menghamba Binasa di atas ditindas Sungguhpun dalam ajal baru tercapai Jika hidup harus merasai Maju. Serbu. Serang. Terjang.
(Diadaptasi dari buku "Aku Ini Binatang Jalang" karya Chairil Anwar)
Struktur lahir yang menonjol dari puisi tersebut adalah ....
Berikut ini yang tidak termasuk bagian-bagian iklan, yaitu ....
Look at the following picture.
Source: wisdomquotesandstories.com
What will you do if you see this?







