Bank Soal Kimia SMA Konsep Kelarutan dan Hasil Kali Kelarutan
Soal
Soal Populer Hari Ini
Dua buah uang logam dilempar secara bersama-sama sebanyak 200 kali. Berapa frekuensi harapan muncul angka?
Matematika
Level 8
Statistika
Peluang
Frekuensi Harapan
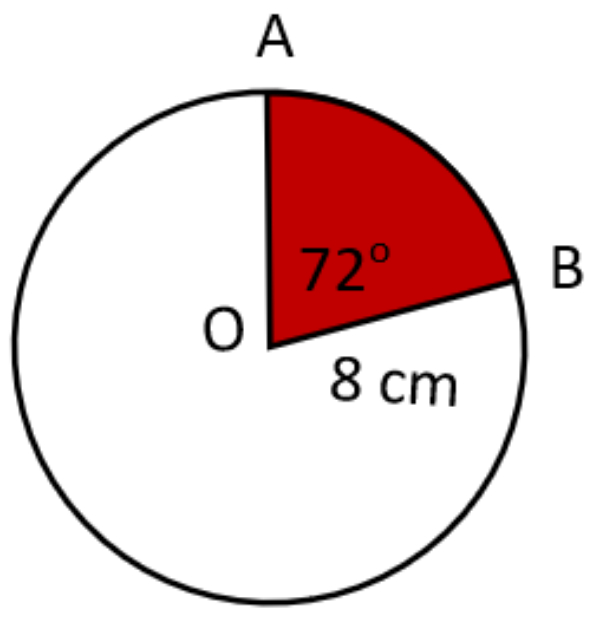
Luas daerah yang berwarna merah adalah ... cm2. ( Gunakan )
Matematika
Level 8
Geometri
Lingkaran
Luas dan Keliling Lingkaran
Perhatikan gambar berikut!
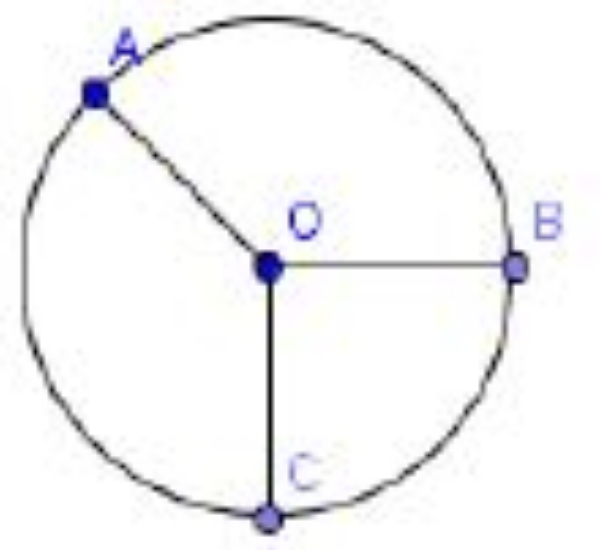
Diketahui panjagn busur AB dan busur BC berturut-turut adalah 33 cm dan 22 cm. Jika luas juring BOC adalah 154 cm2, berapakah luas juring AOB?
Matematika
Level 8
Geometri
Lingkaran
Perhatikanlah gambar koordinat titik di bawah ini!
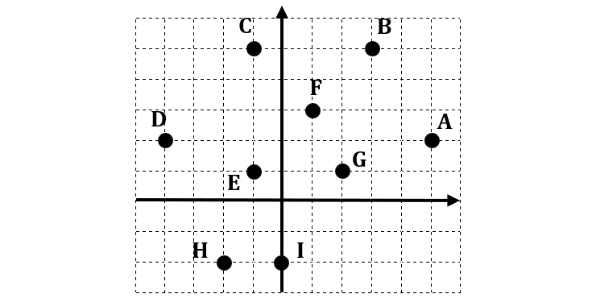
Di antara titik-titik tersebut, titik mana sajakah yang dapat saling membentuk segitiga siku-siku sama kaki?
Matematika
Level 8
Geometri
Koordinat Kartesius
Syarat informasi yang layak diangkat menjadi sebuah berita adalah memiliki sifat ....
Bahasa Indonesia
Level 8
Menulis
Teks Berita
Simpulan Isi Berita
Andy — study — hard — Kate
Which comparative sentence is correct based on the clues above?
Bahasa Inggris
Level 8
Bahasa Inggris
Comparisons of people or things
Degrees of Comparison of Adverbs
Titik A berjarak 8 satuan di sebelah kiri sumbu-Y dan berada di atas sumbu-X dengan jarak setengah dari jaraknya terhadap sumbu-Y.
Berapakah koordinat letak titik A?
Matematika
Level 8
Geometri
Koordinat Kartesius
Koordinat Posisi Suatu Benda
Perhatikan kalimat puisi bermajas di bawah ini!
1) Oh Diana, kembang desa yang memesona
2) Gadis cantik penebar keramahan
3) Menjadi buah bibir masyarakat sejak lama
4) Diana, diana, diana, siapa tidak mendambamu
Kalimat puisi di atas yang mengandung majas metafora adalah kalimat bernomor ....
Bahasa Indonesia
Level 8
Menulis
Puisi
Unsur-unsur puisi
Kementerian Pendidikan dan Kebudayaan membuat sebuah slogan untuk pendidikan Indonesia. Slogan tersebut berbunyi Merdeka Belajar.
Slogan Merdeka Belajar cocok untuk pendidikan Indonesia karena ....
Bahasa Indonesia
Level 8
Menulis
Iklan, Slogan, Poster
Simpulan Isi Iklan, Slogan, Poster
You were asked by your dance art teacher to collect data of students who can dance. The students, later, will be appointed to perform a traditional dance in an art festival next month. When you want to ask Adam, one of your friends, whether he can dance or not, you say ....
Bahasa Inggris
Level 8
Bahasa Inggris
Interaction among students inside and outside classrooms
Expressions of Explaining Abilities
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Dua buah uang logam dilempar secara bersama-sama sebanyak 200 kali. Berapa frekuensi harapan muncul angka?
Luas daerah yang berwarna merah adalah ... cm2. ( Gunakan )
Perhatikan gambar berikut!
Diketahui panjagn busur AB dan busur BC berturut-turut adalah 33 cm dan 22 cm. Jika luas juring BOC adalah 154 cm2, berapakah luas juring AOB?
Perhatikanlah gambar koordinat titik di bawah ini!
Di antara titik-titik tersebut, titik mana sajakah yang dapat saling membentuk segitiga siku-siku sama kaki?
Syarat informasi yang layak diangkat menjadi sebuah berita adalah memiliki sifat ....
Andy — study — hard — Kate
Which comparative sentence is correct based on the clues above?
Titik A berjarak 8 satuan di sebelah kiri sumbu-Y dan berada di atas sumbu-X dengan jarak setengah dari jaraknya terhadap sumbu-Y.
Berapakah koordinat letak titik A?
Perhatikan kalimat puisi bermajas di bawah ini!
1) Oh Diana, kembang desa yang memesona
2) Gadis cantik penebar keramahan
3) Menjadi buah bibir masyarakat sejak lama
4) Diana, diana, diana, siapa tidak mendambamu
Kalimat puisi di atas yang mengandung majas metafora adalah kalimat bernomor ....
Kementerian Pendidikan dan Kebudayaan membuat sebuah slogan untuk pendidikan Indonesia. Slogan tersebut berbunyi Merdeka Belajar.
Slogan Merdeka Belajar cocok untuk pendidikan Indonesia karena ....
You were asked by your dance art teacher to collect data of students who can dance. The students, later, will be appointed to perform a traditional dance in an art festival next month. When you want to ask Adam, one of your friends, whether he can dance or not, you say ....







