Bank Soal Kimia SMA Konsep Kelarutan dan Hasil Kali Kelarutan
Soal
Soal Populer Hari Ini
Populasi tikus di sawah dapat terpengaruh oleh populasi ular. Hal ini menunjukkan permasalahan biologi pada tingkat ....
Biologi
Level 10
Biologi
Ruang Lingkup Biologi
Objek dan Permasalahan Biologi
Choose the correct answer.
Mr. Eddie ... (not/watch) a football match right now.
Bahasa Inggris
Level 10
Congratulating and Complimenting
Tenses: Simple Present & Present Continuous
Metode ilmiah dibangun atas dasar sikap ilmiah dan menghasilkan produk yang tersusun atas tiga komponen terpenting yang berlaku secara universal. Di dalam komponen-komponen tersebut diuraikan lagi mengenai produk fisika. Apa saja produk fisika tersebut?
Fisika
Level 10
Fisika
Hakikat Fisika dan Keselamatan Kerja Laboratorium
Hakikat dan Peran Fisika
Perhatikan gambar berikut!

Sumber: seputarilmu.com
Ketiga spesies di atas termasuk dalam kelompok yang sama, yaitu pada tingkatan takson ....
Biologi
Level 10
Biologi
Keanekaragaman Hayati
Klasifikasi Makhluk Hidup
Nilai pada persamaan adalah ....
Matematika
Level 10
Aljabar
Persamaan dan Pertidaksamaan Nilai Mutlak
Persamaan Linear Satu Variabel
Paragraf pertama termasuk bagian pernyataan umum karena membahas ….
Bahasa Indonesia
Level 10
Teks Laporan Hasil Observasi
Struktur dan Kebahasaan Teks Laporan Hasil Observasi
Fenomena suksesi yang menunjukkan terjadinya kemajuan dalam vegetasi, yaitu ....
Biologi
Level 10
Biologi
Ekologi
Dinamika Komunitas
Diketahui
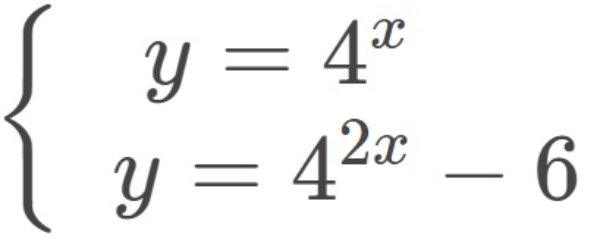
Himpunan penyelesaian untuk sistem persamaan dua variabel di atas adalah ....
Matematika
Level 10
Aljabar
Sistem Pertidaksamaan Dua Variabel
Sistem Persamaan Dua Variabel
Perhatikan gambar berikut!
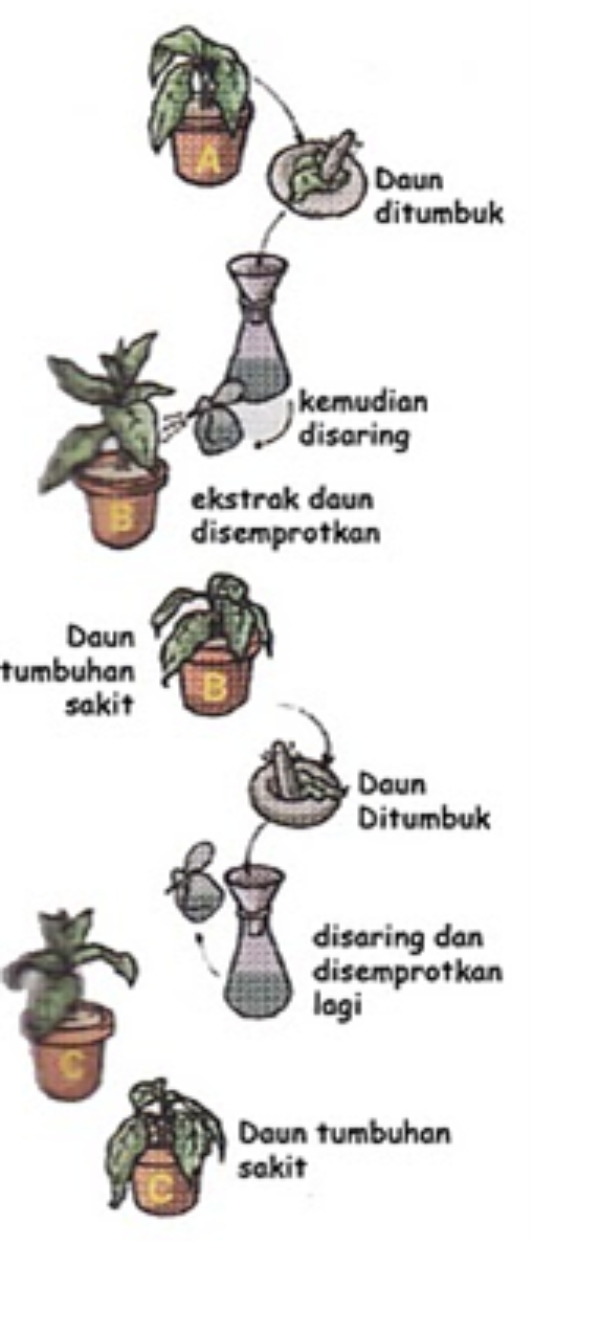
sumber: almansyahnis.com
Penelitian pada tembakau seperti gambar di atas dilakukan oleh ....
Biologi
Level 10
Biologi
Virus
Sejarah Virus
Pencampuran serbuk besi dan serbuk belerang pada suhu tinggi menghasilkan suatu zat berwarna hitam. Maka, zat tersebut digolongkan sebagai ....
Kimia
Level 10
Perkenalan Ilmu Kimia
Materi dan Klasifikasinya
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Populasi tikus di sawah dapat terpengaruh oleh populasi ular. Hal ini menunjukkan permasalahan biologi pada tingkat ....
Choose the correct answer.
Mr. Eddie ... (not/watch) a football match right now.
Metode ilmiah dibangun atas dasar sikap ilmiah dan menghasilkan produk yang tersusun atas tiga komponen terpenting yang berlaku secara universal. Di dalam komponen-komponen tersebut diuraikan lagi mengenai produk fisika. Apa saja produk fisika tersebut?
Perhatikan gambar berikut!
Sumber: seputarilmu.com
Ketiga spesies di atas termasuk dalam kelompok yang sama, yaitu pada tingkatan takson ....
Nilai pada persamaan adalah ....
Paragraf pertama termasuk bagian pernyataan umum karena membahas ….
Fenomena suksesi yang menunjukkan terjadinya kemajuan dalam vegetasi, yaitu ....
Diketahui
Himpunan penyelesaian untuk sistem persamaan dua variabel di atas adalah ....
Perhatikan gambar berikut!
sumber: almansyahnis.com
Penelitian pada tembakau seperti gambar di atas dilakukan oleh ....
Pencampuran serbuk besi dan serbuk belerang pada suhu tinggi menghasilkan suatu zat berwarna hitam. Maka, zat tersebut digolongkan sebagai ....







