Bank Soal Kimia SMA Nilai pH Larutan Garam
Soal
LOTS
Soal Populer Hari Ini
Bagaimanakah cara mengerjakan soal ini?
Matematika
Level 5
Bilangan
Operasi Hitung Pecahan
Operasi Hitung Pecahan Biasa dan Campuran
Kelas V
Kurikulum 2013
K13
Matematika
Paman mengendarai mobil dengan kecepatan 50 km/jam. Jika paman berangkat pukul 07.30 dan tiba pukul 10.00. Jarak yang ditempuh paman yaitu …
Matematika
Level 5
Geometri
Perbandingan Dua Besaran
Kecepatan
Kelas V
Kurikulum 2013
K13
Matematika
Berdasarkan isinya, kelompok yang tidak termasuk ke dalam iklan elektronik yaitu ....
Bahasa Indonesia
Level 5
Membaca
Iklan
Jenis-jenis Iklan
Perhatikan diagram berikut!
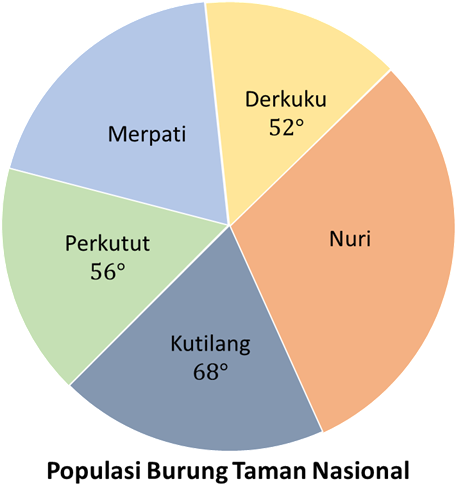
Pernyataan yang sesuai dengan diagram di atas adalah ...
Matematika
Level 5,16
Statistika
Pengumpulan dan Penyajian Data
Membaca Data
AKM
Asesmen Kompetensi Minimum
Saintifik
Data dan Ketidakpastian
Numerasi
Menafsirkan
Level 3
Seorang pebisnis telur ingin mengecek produksi telur. Diagram berikut menunjukkan hasil produksi telur dari bulan Januari hingga Juni.
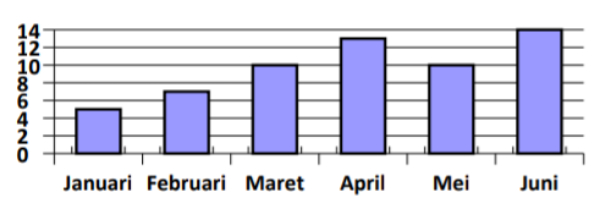
Produksi telur yang lebih dari 10 kuintal terjadi pada bulan ....
Matematika
Level 5,16
Statistika
Pengumpulan dan Penyajian Data
Membaca Data
AKM
Asesmen Kompetensi Minimum
Personal
Data dan Ketidakpastian
Numerasi
Mengambil/Memperoleh
Level 3
Perhatikan gambar!
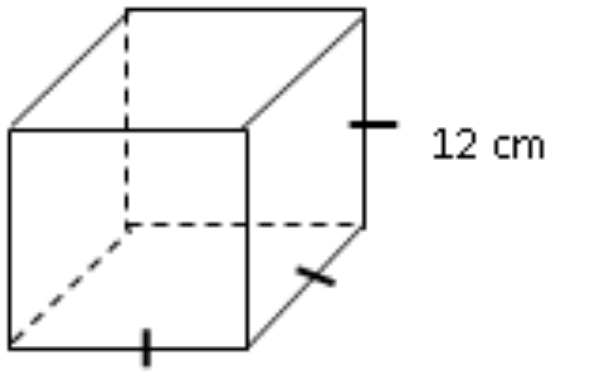
Mira akan membungkus kado yang berbentuk kubus seperti gambar. Luas kertas kado minimal yang dibutuhkan Mira adalah ....
Matematika
Level 5
Geometri
Balok dan Kubus
Luas Permukaan Balok dan Kubus
Kelas V
Kurikulum 2013
K13
Matematika
Read the text below. Then, fill in the blank with a correct verb to be.

Source: creazilla.com
My name is Claire. I live in Arizona. I am in fifth grade. I have a brother. His name is Peter. He is in fourth grade.
Based on the text, we know that Claire and Peter ... students.
Bahasa Inggris
Level 5
Bahasa Inggris
Friendship
Self-Introduction
Kelas V
Kurikulum 2013
K13
Ide pokok paragraf ketiga adalah ....
Bahasa Indonesia
Level 5
Membaca
Teks Eksplanasi
Struktur Teks Eksplanasi
(1) Surat pengumuman
(2) Surat perizinan
(3) Undangan ulang tahun
(4) Undangan khitanan
Yang termasuk surat undangan tidak resmi adalah nomor ….
Bahasa Indonesia
Level 5
Membaca
Surat Undangan
Identifikasi Surat Undangan
Ciri yang menunjukkan Indonesia sebagai negara maritim adalah ....
IPS
Level 5
Geografi
Karakteristik Geografi Wilayah Indonesia
Karakteristik Geografis
Kelas V
Kurikulum 2013
K13
IPS
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Bagaimanakah cara mengerjakan soal ini?
Paman mengendarai mobil dengan kecepatan 50 km/jam. Jika paman berangkat pukul 07.30 dan tiba pukul 10.00. Jarak yang ditempuh paman yaitu …
Berdasarkan isinya, kelompok yang tidak termasuk ke dalam iklan elektronik yaitu ....
Perhatikan diagram berikut!
Pernyataan yang sesuai dengan diagram di atas adalah ...
Seorang pebisnis telur ingin mengecek produksi telur. Diagram berikut menunjukkan hasil produksi telur dari bulan Januari hingga Juni.
Produksi telur yang lebih dari 10 kuintal terjadi pada bulan ....
Perhatikan gambar!
Mira akan membungkus kado yang berbentuk kubus seperti gambar. Luas kertas kado minimal yang dibutuhkan Mira adalah ....
Read the text below. Then, fill in the blank with a correct verb to be.

Source: creazilla.com
My name is Claire. I live in Arizona. I am in fifth grade. I have a brother. His name is Peter. He is in fourth grade.
Based on the text, we know that Claire and Peter ... students.
Ide pokok paragraf ketiga adalah ....
(1) Surat pengumuman
(2) Surat perizinan
(3) Undangan ulang tahun
(4) Undangan khitanan
Yang termasuk surat undangan tidak resmi adalah nomor ….
Ciri yang menunjukkan Indonesia sebagai negara maritim adalah ....







