Bank Soal Kimia SMA Stoikiometri Persamaan Reaksi
Soal
LOTS
Soal Populer Hari Ini
sama dengan ...
Pilih semua jawaban yang benar.
Matematika
Level 4
Bilangan
Pecahan
Bentuk Pecahan
Rumus luas jajar genjang yaitu …
Matematika
Level 5,6
Geometri
Bangun Datar
Di bawah ini adalah unsur-unsur yang terdapat di dalam sebuah karya sastra, kecuali ....
Bahasa Indonesia
Level 4
Membaca
Buku Sastra
Ulasan Buku Sastra

Fill in the blank with the correct verb.
She is a dancer. She ____ on the stage.
Bahasa Inggris
Level 4
Bahasa Inggris
Jobs
Simple Present Tense
Faktor dari 48 adalah ...
Matematika
Level 4
Bilangan
Faktor dan Kelipatan
Faktor Bilangan
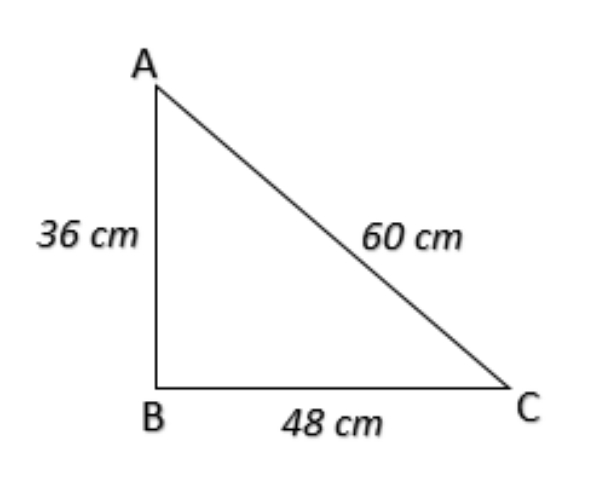
Keliling segitiga di atas adalah ... cm
Matematika
Level 4
Geometri
Bangun Datar
Keliling dan Luas Segitiga
Bilangan prima antara 1 sampai 10 adalah ...
Matematika
Level 4
Bilangan
FPB dan KPK
Faktor dan Faktorisasi Prima
Cermati teks berikut!
Siasat Bangau Tua

Alkisah hiduplah seekor bangau tua di pinggir sebuah telaga. Karena usianya sudah tua, ia tidak dapat lagi menangkap mangsanya di telaga sebanyak dulu lagi. Akibatnya, tubuhnya mengurus. Ia pun mencari akal untuk mendapatkan makanan supaya ia tidak mati kelaparan.
Pagi itu ia melaksanakan rencana yang sudah dipikirkannya semalaman. Ia duduk termenung di pinggir telaga dengan raut muka sedih. Ikan-ikan yang lewat di dekatnya pun tidak berusaha ditangkap seperti biasanya. Tindak tanduknya ini pun jadi pembicaraan hewan-hewan yang hidup di telaga. Akhirnya seekor katak penasaran dan menghampirinya,"Mengapa kamu terlihat sangat sedih dan tidak lagi memburu kami?" Jawab bangau,"Aku bersedih karena para manusia yang tinggal di sekitar telaga berencana untuk menimbun telaga dengan tanah. Kalau itu terjadi, semua makhluk dalam telaga akan mati. Aku pun akan mati kelaparan karenanya. Karena itu aku merasa sangat sedih."
Katak sangat terkejut mendengar hal ini dan segera memberitahukannya ke hewan-hewan lainnya di dalam telaga. Tak lama kemudian semua hewan di telaga telah mendengarnya dan merasa panik. Mereka mendatangi bangau untuk minta bantuan. Usul bangau,"Aku tahu ada telaga lain di dekat sini. Aku bisa mengantar kalian ke sana sebelum telaga ini ditimbun tanah. Tapi karena sudah tua, aku hanya bisa mengangkat satu hewan sekali jalan." Segera para hewan telaga menyetujuinya.
Sore itu ia mulai membawa hewan telaga satu per satu, dimulai dari ikan. Begitu sampai di tempat aman yang tak terlihat dari telaga, segera ia telan ikan itu. Lalu ia kembali lagi untuk mengambil ikan berikutnya hingga ia merasa kenyang. Hari demi hari tubuhnya semakin gemuk.
Suatu hari seekor kepiting meminta bangau untuk membawanya ke telaga sebelah. Bangau pun menyanggupinya. Ia terbang dengan membawa kepiting di paruhnya. Namun ketika akan hinggap di tempat biasanya, sang kepiting melihat tulang-tulang ikan yang berserakan. Ia langsung menyadari apa yang terjadi, dan mengancam bangau dengan melingkari lehernya dengan capitnya yang besar. Lalu ia usir sang bangau dan ia ceritakan jebakan bangau kepada hewan-hewan telaga. Para hewan telaga berterima kasih pada kepiting dan mengusungnya sebagai pahlawan.
Amanat yang terdapat pada cerita di atas adalah ....
Bahasa Indonesia
Level 4
Membaca
Teks Fiksi-Tokoh Cerita
Dongeng
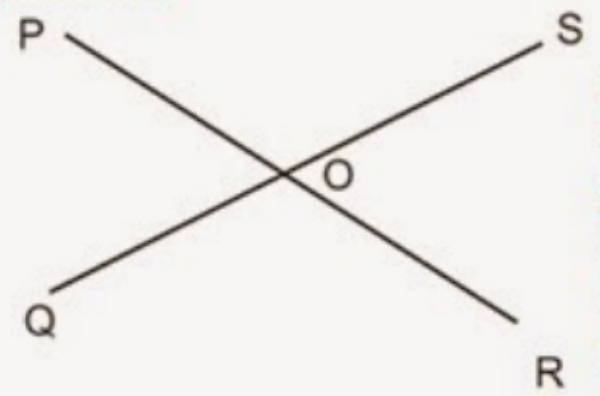
Bila POQ adalah 50, maka besar QOR adalah ....
Matematika
Level 4
Geometri
Garis dan Sudut
Sudut
sama dengan ...
Pilih semua jawaban yang benar.
Matematika
Level 4
Bilangan
Pecahan
Bentuk Pecahan
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
sama dengan ...
Pilih semua jawaban yang benar.
Rumus luas jajar genjang yaitu …
Di bawah ini adalah unsur-unsur yang terdapat di dalam sebuah karya sastra, kecuali ....

Fill in the blank with the correct verb.
She is a dancer. She ____ on the stage.
Faktor dari 48 adalah ...
Keliling segitiga di atas adalah ... cm
Bilangan prima antara 1 sampai 10 adalah ...
Cermati teks berikut!
Siasat Bangau Tua
Alkisah hiduplah seekor bangau tua di pinggir sebuah telaga. Karena usianya sudah tua, ia tidak dapat lagi menangkap mangsanya di telaga sebanyak dulu lagi. Akibatnya, tubuhnya mengurus. Ia pun mencari akal untuk mendapatkan makanan supaya ia tidak mati kelaparan.
Pagi itu ia melaksanakan rencana yang sudah dipikirkannya semalaman. Ia duduk termenung di pinggir telaga dengan raut muka sedih. Ikan-ikan yang lewat di dekatnya pun tidak berusaha ditangkap seperti biasanya. Tindak tanduknya ini pun jadi pembicaraan hewan-hewan yang hidup di telaga. Akhirnya seekor katak penasaran dan menghampirinya,"Mengapa kamu terlihat sangat sedih dan tidak lagi memburu kami?" Jawab bangau,"Aku bersedih karena para manusia yang tinggal di sekitar telaga berencana untuk menimbun telaga dengan tanah. Kalau itu terjadi, semua makhluk dalam telaga akan mati. Aku pun akan mati kelaparan karenanya. Karena itu aku merasa sangat sedih."
Katak sangat terkejut mendengar hal ini dan segera memberitahukannya ke hewan-hewan lainnya di dalam telaga. Tak lama kemudian semua hewan di telaga telah mendengarnya dan merasa panik. Mereka mendatangi bangau untuk minta bantuan. Usul bangau,"Aku tahu ada telaga lain di dekat sini. Aku bisa mengantar kalian ke sana sebelum telaga ini ditimbun tanah. Tapi karena sudah tua, aku hanya bisa mengangkat satu hewan sekali jalan." Segera para hewan telaga menyetujuinya.
Sore itu ia mulai membawa hewan telaga satu per satu, dimulai dari ikan. Begitu sampai di tempat aman yang tak terlihat dari telaga, segera ia telan ikan itu. Lalu ia kembali lagi untuk mengambil ikan berikutnya hingga ia merasa kenyang. Hari demi hari tubuhnya semakin gemuk.
Suatu hari seekor kepiting meminta bangau untuk membawanya ke telaga sebelah. Bangau pun menyanggupinya. Ia terbang dengan membawa kepiting di paruhnya. Namun ketika akan hinggap di tempat biasanya, sang kepiting melihat tulang-tulang ikan yang berserakan. Ia langsung menyadari apa yang terjadi, dan mengancam bangau dengan melingkari lehernya dengan capitnya yang besar. Lalu ia usir sang bangau dan ia ceritakan jebakan bangau kepada hewan-hewan telaga. Para hewan telaga berterima kasih pada kepiting dan mengusungnya sebagai pahlawan.
Amanat yang terdapat pada cerita di atas adalah ....
Bila POQ adalah 50, maka besar QOR adalah ....
sama dengan ...
Pilih semua jawaban yang benar.







