Bank Soal Kimia SMA Nilai pH Larutan Garam
Soal
LOTS Memahami
Soal Populer Hari Ini
Dua buah uang logam dilempar secara bersama-sama sebanyak 48 kali. Berapa frekuensi harapan muncul 2 gambar?
Matematika
Level 8
Statistika
Peluang
Frekuensi Harapan
Kakak mempunyai tali berbentuk lingkaran dengan panjang jari-jari 7 cm, sedangkan adik mempunyai tali berbentuk lingkaran dengan panjang jari-jari 3,5 cm. Perbandingan panjang tali kakak terhadap adik adalah ...
Matematika
Level 8
Geometri
Lingkaran
Luas dan Keliling Lingkaran
Pada gambar di bawah ini, jika keliling lingkaran 90 cm, panjang busur AD = 20 cm, dan panjang busur BC = 10 cm, tentukan besar sudut ATD!
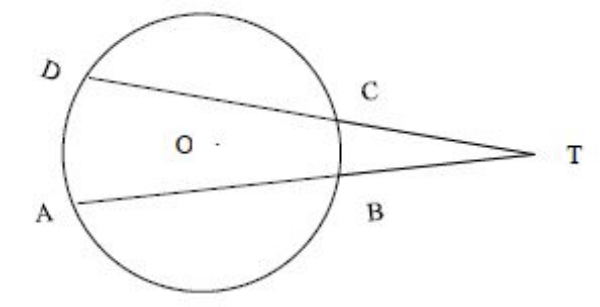
Matematika
Level 8
Geometri
Lingkaran
Diantara titik berikut yang mempunyai jarak 8 satuan terhadap sumbu-y adalah?
Matematika
Level 8
Geometri
Koordinat Kartesius
Bacalah penggalan paragraf berikut!
Susan L. Hymen, pediatris khusus penanganan tumbuh kembang anak dari Rochester University mengatakan bahwa semakin dini seorang anak terdiagnosa keterlambatan tumbuh kembang, maka kian cepat dapat teratasi masalahnya, sehingga dapat mengantisipasi kondisi tertentu.
(Sumber: difabel.tempo.co)
Kalimat tidak langsung tersebut diubah menjadi kalimat langsung menjadi ....
Bahasa Indonesia
Level 8
Menulis
Teks Berita
Struktur dan Kebahasaan Teks Berita
Bella — shop — frequent — Nia
Which comparative sentence is correct based on the clues above?
Bahasa Inggris
Level 8
Bahasa Inggris
Comparisons of people or things
Degrees of Comparison of Adverbs
Perhatikan gambar di bawah ini.

Dika bermula di posisi A. Kemudian dia berjalan 5 langkah ke kanan dan dilanjutkan 2 langkah ke atas. Koordinat Dika saat ini adalah ....
Matematika
Level 8
Geometri
Koordinat Kartesius
Koordinat Posisi Suatu Benda
Yang termasuk unsur ekstrinsik dari pembuatan puisi adalah ....
Bahasa Indonesia
Level 8
Menulis
Puisi
Unsur-unsur puisi
Kedai Minuman Rina
Rina akan membuka kedai minuman kekinian minggu depan. Ia membuat poster untuk mempromosikan kedai tersebut. Perhatikan poster kedai minuman milik Rina di bawah ini!

(Sumber Gambar: foodyas.com)
Di mana kamu bisa mendapatkan informasi lebih lanjut tentang kedai minuman milik Rina?
Bahasa Indonesia
Level 8
Menulis
Iklan, Slogan, Poster
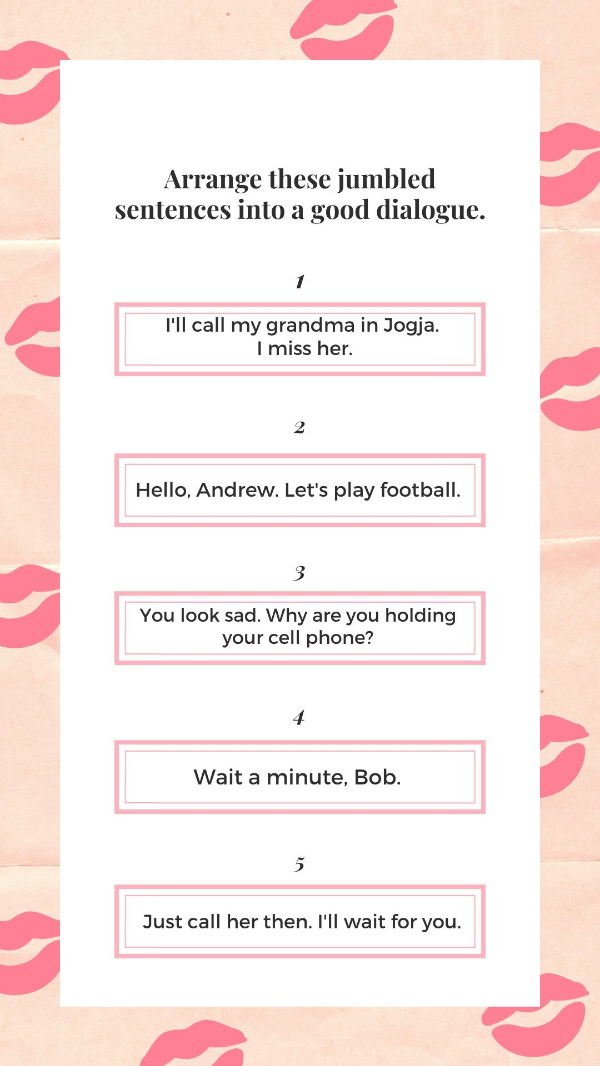
Source: canva.com
What's the best arrangement for the dialogue?
Bahasa Inggris
Level 8
Bahasa Inggris
Interaction among students inside and outside classrooms
Expressions of Willingness to Do Something
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Dua buah uang logam dilempar secara bersama-sama sebanyak 48 kali. Berapa frekuensi harapan muncul 2 gambar?
Kakak mempunyai tali berbentuk lingkaran dengan panjang jari-jari 7 cm, sedangkan adik mempunyai tali berbentuk lingkaran dengan panjang jari-jari 3,5 cm. Perbandingan panjang tali kakak terhadap adik adalah ...
Pada gambar di bawah ini, jika keliling lingkaran 90 cm, panjang busur AD = 20 cm, dan panjang busur BC = 10 cm, tentukan besar sudut ATD!
Diantara titik berikut yang mempunyai jarak 8 satuan terhadap sumbu-y adalah?
Bacalah penggalan paragraf berikut!
Susan L. Hymen, pediatris khusus penanganan tumbuh kembang anak dari Rochester University mengatakan bahwa semakin dini seorang anak terdiagnosa keterlambatan tumbuh kembang, maka kian cepat dapat teratasi masalahnya, sehingga dapat mengantisipasi kondisi tertentu.
(Sumber: difabel.tempo.co)
Kalimat tidak langsung tersebut diubah menjadi kalimat langsung menjadi ....
Bella — shop — frequent — Nia
Which comparative sentence is correct based on the clues above?
Perhatikan gambar di bawah ini.
Dika bermula di posisi A. Kemudian dia berjalan 5 langkah ke kanan dan dilanjutkan 2 langkah ke atas. Koordinat Dika saat ini adalah ....
Yang termasuk unsur ekstrinsik dari pembuatan puisi adalah ....
Kedai Minuman Rina
Rina akan membuka kedai minuman kekinian minggu depan. Ia membuat poster untuk mempromosikan kedai tersebut. Perhatikan poster kedai minuman milik Rina di bawah ini!
(Sumber Gambar: foodyas.com)
Di mana kamu bisa mendapatkan informasi lebih lanjut tentang kedai minuman milik Rina?
Source: canva.com
What's the best arrangement for the dialogue?







