Bank Soal Kimia SMA Pengaruh Ion Senama pada Kelarutan
Soal
LOTS
Soal Populer Hari Ini
Ibu ingin berbelanja bahan makanan untuk dapur di rumah dengan rincian:
1) Belanja beras (B) tidak lebih dari Rp75.000,00
2) Belanja ayam (A) maksimal Rp45.000,00
3) Belanja tempe (T) tidak melebihi Rp12.000,00
Jika jumlah uang yang dibawa Ibu (X) adalah Rp150.000,00, maka kalimat matematika berikut yang tepat adalah ....
Matematika
Level 7
Aljabar
Persamaan dan Pertidaksamaan Linear Satu Variabel
Pertidaksamaan Linear Satu Variabel (PtLSV)
(i) (-50)2 -32 + 23 = 0
(ii) -82 : (22)3 = 20
(iii) 73 - 35 = 102
Pernyataan yang tepat adalah ...
Matematika
Level 7
Bilangan
Bilangan dan Operasi Hitung Bilangan
Bilangan Berpangkat
Pak Arif, Pak Bagus, dan Pak Chiko adalah penduduk Desa Bahagia yang pekerjaannya bertani. Pak Arif menanam singkong, padi, dan kentang; Pak Bagus menanam talas, kentang, dan jagung; Pak Chiko menanam singkong dan kentang. Himpunan semua jenis tanaman penduduk Desa Bahagia yang bertani adalah …
Matematika
Level 7
Bilangan
Himpunan
Konsep dan Macam-Macam Himpunan
Ruas garis AH dibagi menjadi 9 bagian sama panjang seperti gambar berikut.

Perbandingan antara panjang NU dan LQ adalah ....
Matematika
Level 7
Geometri
Garis dan Sudut
Perbandingan Ruas Garis
Berikut ini yang tidak terdapat pada bagian identifikasi teks deskripsi adalah ….
Bahasa Indonesia
Level 7
Menulis
Teks Deskripsi
Struktur dan Kebahasaan Teks Deskripsi
Hasil dari:
Matematika
Level 7
Aljabar
Bentuk Aljabar
Operasi Hitung Bentuk Aljabar
Jika di dalam surat dinas ada kop surat, maka bagian yang tidak perlu dicantumkan adalah ....
Bahasa Indonesia
Level 7
Menulis
Surat Pribadi dan Surat Dinas
Unsur-unsur dan Kebahasaan Surat
Perhatikan biografi berikut!

(Sumber gambar: akurat.co)
Salah satu penyanyi Indonesia yang pernah berduet dengan banyak penyanyi kenamaan Indonesia adalah Iwan Fals. Beliau pernah membawakan lagu berjudul Percayalah Kasih bersama Jockie Surjoprajogo dan Vina Panduwinata. Penyanyi dengan nama asli Virgiawan Lisanto ini merupakan salah satu legenda di Indonesia. Gaya musik yang dibawakannya adalah pop, rock, country, hingga folk pop. Lirik dari lagu-lagu Iwan Fals banyak menceritakan masa-masa kelam era 1970 hingga 1980-an di bidang politik. Salah satu lagunya bersama Swarmi yang berjudul Bongkar menerima penghargaan 150 lagu terbaik sepanjang masa versi Majalah Rolling Stone peringkat 1.
(Dikutip dari berbagai sumber)
Di bawah ini merupakan gaya musik yang dibawakan oleh Iwan Fals, kecuali ….
Bahasa Indonesia
Level 7
Menulis
Buku Fiksi dan Nonfiksi
Unsur Pembangun Buku Fiksi dan Nonfiksi
Diagram garis ini menyajikan jumlah tabungan Maria selama satu tahun.
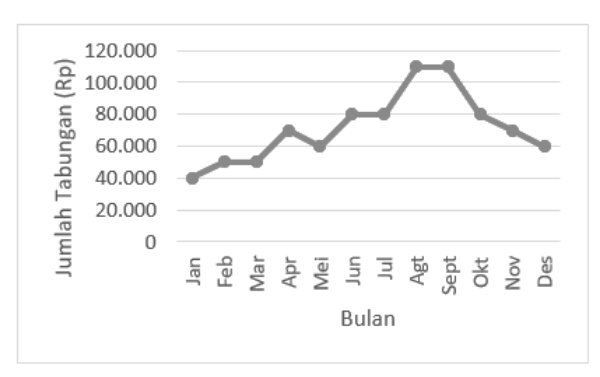
Tabungan Maria pada bulan April ada …
Matematika
Level 5
Statistika
Penyajian dan Pengolahan Data
Penyajian dan Pengolahan Data
We say 'What do you do' when we want to know someone's ....
Bahasa Inggris
Level 7
Bahasa Inggris
Describing oneself
Self Introduction
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Ibu ingin berbelanja bahan makanan untuk dapur di rumah dengan rincian:
1) Belanja beras (B) tidak lebih dari Rp75.000,00
2) Belanja ayam (A) maksimal Rp45.000,00
3) Belanja tempe (T) tidak melebihi Rp12.000,00
Jika jumlah uang yang dibawa Ibu (X) adalah Rp150.000,00, maka kalimat matematika berikut yang tepat adalah ....
(i) (-50)2 -32 + 23 = 0
(ii) -82 : (22)3 = 20
(iii) 73 - 35 = 102
Pernyataan yang tepat adalah ...
Pak Arif, Pak Bagus, dan Pak Chiko adalah penduduk Desa Bahagia yang pekerjaannya bertani. Pak Arif menanam singkong, padi, dan kentang; Pak Bagus menanam talas, kentang, dan jagung; Pak Chiko menanam singkong dan kentang. Himpunan semua jenis tanaman penduduk Desa Bahagia yang bertani adalah …
Ruas garis AH dibagi menjadi 9 bagian sama panjang seperti gambar berikut.
Perbandingan antara panjang NU dan LQ adalah ....
Berikut ini yang tidak terdapat pada bagian identifikasi teks deskripsi adalah ….
Hasil dari:
Jika di dalam surat dinas ada kop surat, maka bagian yang tidak perlu dicantumkan adalah ....
Perhatikan biografi berikut!
(Sumber gambar: akurat.co)
Salah satu penyanyi Indonesia yang pernah berduet dengan banyak penyanyi kenamaan Indonesia adalah Iwan Fals. Beliau pernah membawakan lagu berjudul Percayalah Kasih bersama Jockie Surjoprajogo dan Vina Panduwinata. Penyanyi dengan nama asli Virgiawan Lisanto ini merupakan salah satu legenda di Indonesia. Gaya musik yang dibawakannya adalah pop, rock, country, hingga folk pop. Lirik dari lagu-lagu Iwan Fals banyak menceritakan masa-masa kelam era 1970 hingga 1980-an di bidang politik. Salah satu lagunya bersama Swarmi yang berjudul Bongkar menerima penghargaan 150 lagu terbaik sepanjang masa versi Majalah Rolling Stone peringkat 1.
(Dikutip dari berbagai sumber)
Di bawah ini merupakan gaya musik yang dibawakan oleh Iwan Fals, kecuali ….
Diagram garis ini menyajikan jumlah tabungan Maria selama satu tahun.
Tabungan Maria pada bulan April ada …
We say 'What do you do' when we want to know someone's ....