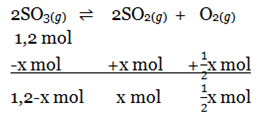Bank Soal Kimia SMA Hukum, Tetapan, dan Pergeseran Kesetimbangan
Soal
LOTS
Soal Populer Hari Ini
Frekuensi harapan muncul mata dadu bilangan prima pada pelemparan sebuah dadu adalah 120 kali. Berapa banyak lemparan yang dilakukan?
Matematika
Level 8
Statistika
Peluang
Frekuensi Harapan
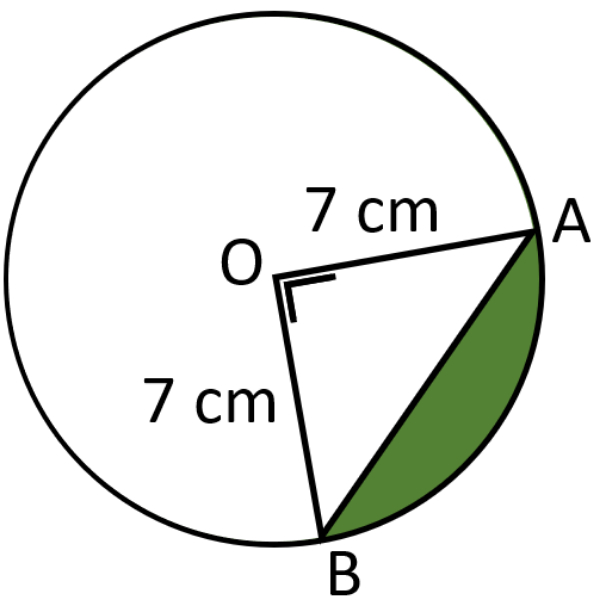
Luas daerah yang berwarna hijau adalah ... cm2 ( Gunakan = )
Matematika
Level 8
Geometri
Lingkaran
Luas dan Keliling Lingkaran
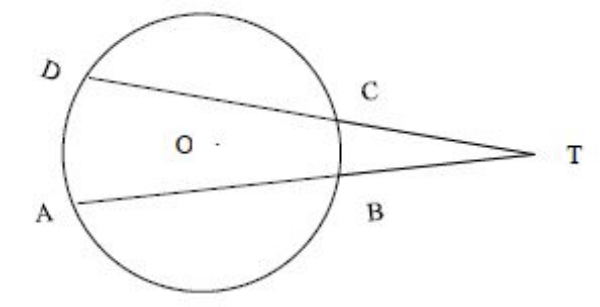
Pada gambar di bawah ini, jika keliling lingkaran 90 cm, panjang busur AD = 20 cm, dan panjang busur BC = 10 cm, tentukan besar sudut ATD!
Matematika
Level 8
Geometri
Lingkaran
Adit, Baba, Cahyo, dan Dedi tengah duduk di sebuah bangku pada suatu lorong. Adit duduk di posisi kedua dari kanan dan bersebelahan dengan Baba. Cahyo dan Dedi masing-masing berada diposisi ujung bangku. Jika Cahyo dan Baba mengapit Adit, maka ketika Ella datang, dimanakah posisi Ella saat duduk dibangku yang sama?
Matematika
Level 8
Geometri
Koordinat Kartesius
Pengertian berita adalah ....
Bahasa Indonesia
Level 8
Menulis
Teks Berita
Unsur-unsur Berita
Read the following teacher’s talk.

Source: shutterstock.com
"Well done, everyone. You did your best in your English speech today. However, some of you still need to speak more confidently."
The comparison form of “more confidently” refers to ….
Bahasa Inggris
Level 8
Bahasa Inggris
Comparisons of people or things
Degrees of Comparison of Adverbs
Coba perhatikan gambar denah lingkungan komplek Pertama Hijau pada bidang koordinat dua dimensi berikut!

Bagaimanakah posisi rumah Rina terhadap kolam renang?
Matematika
Level 8
Geometri
Koordinat Kartesius
Koordinat Posisi Suatu Benda
Cermati pilihan berikut!
- Tema
- Diksi
- Rasa
- Imaji
- Tipografi
- Amanat
Yang termasuk di dalam struktur lahir sebagai unsur pembangun sebuah puisi adalah nomor ....
Bahasa Indonesia
Level 8
Menulis
Puisi
Unsur-unsur puisi
Perhatikan iklan berikut!

(Sumber gambar: contohsurat.co dengan penyesuaian)
Iklan tersebut menginformasikan bahwa ....
Bahasa Indonesia
Level 8
Menulis
Iklan, Slogan, Poster
Unsur-unsur Iklan, Slogan, Poster
You are about going to the bookstore to buy some novels. Suddenly, you meet your classmate on the way you go to the bookstore. You want to ask him whether he is willing to come with you to the bookstore or not. You may say ....
Bahasa Inggris
Level 8
Bahasa Inggris
Interaction among students inside and outside classrooms
Expressions of Willingness to Do Something
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Frekuensi harapan muncul mata dadu bilangan prima pada pelemparan sebuah dadu adalah 120 kali. Berapa banyak lemparan yang dilakukan?
Luas daerah yang berwarna hijau adalah ... cm2 ( Gunakan = )
Pada gambar di bawah ini, jika keliling lingkaran 90 cm, panjang busur AD = 20 cm, dan panjang busur BC = 10 cm, tentukan besar sudut ATD!
Adit, Baba, Cahyo, dan Dedi tengah duduk di sebuah bangku pada suatu lorong. Adit duduk di posisi kedua dari kanan dan bersebelahan dengan Baba. Cahyo dan Dedi masing-masing berada diposisi ujung bangku. Jika Cahyo dan Baba mengapit Adit, maka ketika Ella datang, dimanakah posisi Ella saat duduk dibangku yang sama?
Pengertian berita adalah ....
Read the following teacher’s talk.

Source: shutterstock.com
"Well done, everyone. You did your best in your English speech today. However, some of you still need to speak more confidently."
The comparison form of “more confidently” refers to ….
Coba perhatikan gambar denah lingkungan komplek Pertama Hijau pada bidang koordinat dua dimensi berikut!
Bagaimanakah posisi rumah Rina terhadap kolam renang?
Cermati pilihan berikut!
- Tema
- Diksi
- Rasa
- Imaji
- Tipografi
- Amanat
Yang termasuk di dalam struktur lahir sebagai unsur pembangun sebuah puisi adalah nomor ....
Perhatikan iklan berikut!
(Sumber gambar: contohsurat.co dengan penyesuaian)
Iklan tersebut menginformasikan bahwa ....
You are about going to the bookstore to buy some novels. Suddenly, you meet your classmate on the way you go to the bookstore. You want to ask him whether he is willing to come with you to the bookstore or not. You may say ....