Bank Soal Kimia SMA Pengaruh Ion Senama pada Kelarutan
Soal
Soal Populer Hari Ini
Kelompok lipid yang terlibat dalam penyusun lapisan kutikula pada permukaan daun tanaman adalah ....
Biologi
Level 11
Biologi
Sel
Penemuan, Tipe, Ukuran, dan Komponen Kimiawi Sel
Bayangan garis oleh translasi 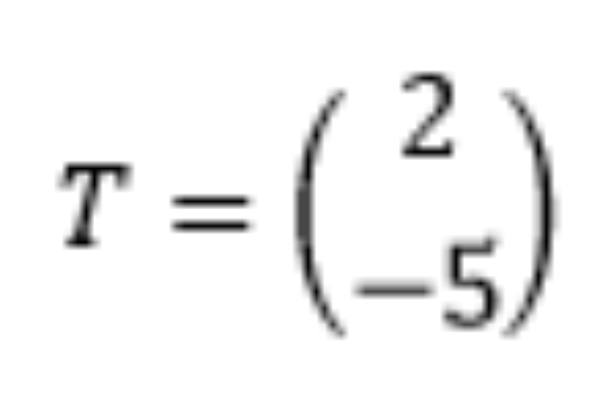 adalah ....
adalah ....
Matematika
Level 11
Geometri
Transformasi Geometri
Tranlasi
Why does Elsa can’t study seriously?
Bahasa Inggris
Level 11
Good Advice
Giving Advice or Suggestions
Di antara senyawa berikut yang bukan merupakan isomer dari 2,4-dimetiloktana adalah ....
Kimia
Level 11
Hidrokarbon dan Minyak Bumi
Hidrokarbon
Diketahui adalah rumus dari
Jika benar untuk , maka ruas kiri menjadi ....
Matematika
Level 11
Logika
Induksi Matematika
Induksi Matematika pada Barisan Bilangan
Pernyataan yang benar tentang momen inersia adalah ....
Fisika
Level 11
Fisika
Dinamika dan Keseimbangan Benda Tegar
Dinamika Benda Tegar
Suatu gas propana direaksikan dengan gas klorin dan dihasilkan senyawa X. Senyawa X yang dimaksud adalah ....
Kimia
Level 11
Hidrokarbon dan Minyak Bumi
Hidrokarbon
Jenis endositosis yang terjadi dimana sel "meneguk" tetesan fluida ekstraseluler dalam vesikula kecil disebut juga dengan ....
Biologi
Level 11
Biologi
Sel
Mekanisme Transpor Membran Plasma
Himpunan penyelesaian dari persamaan trigonometri dengan adalah ....
Matematika
Level 11
Trigonometri
Persamaan Trigonometri
Perhatikan tabel emisi karbon dioksida yang disebabkan berbagai pembangkit listrik berikut!

Sebuah kantor kecil di kawasan SCBD memiliki komputer sebanyak 10 unit, mesin fotokopi sebanyak 1 unit, dispenser sebanyak 2 unit, proyektor sebanyak 3 unit, dan AC sebanyak 4 unit. Konsumsi daya serta lama waktu pemakian rata-rata harian dari masing-masing peralatan kantor tersebut adalah

Diketahui bahwa kantor-kantor di kawasan SCBD disuplai oleh PLTU Muara Karang yang menggunakan batu bara jenis bituminous sebagai sumber energinya. Berapa besar kontribusi karbon dioksida yang dihasilkan oleh kantor tersebut setiap harinya?
Fisika
Level 11
Fisika
Pemanasan Global
Pemanasan Global dan Efek Rumah Kaca
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Kelompok lipid yang terlibat dalam penyusun lapisan kutikula pada permukaan daun tanaman adalah ....
Bayangan garis oleh translasi 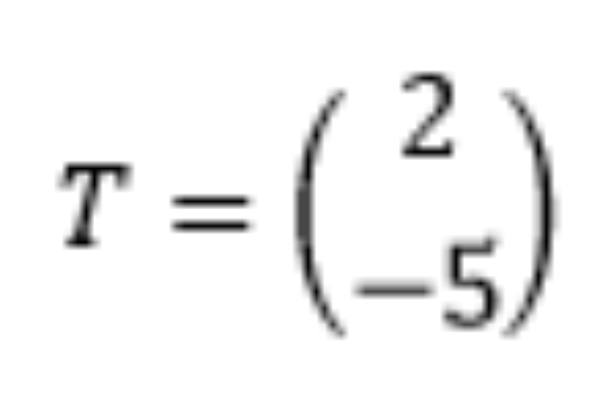
Why does Elsa can’t study seriously?
Di antara senyawa berikut yang bukan merupakan isomer dari 2,4-dimetiloktana adalah ....
Diketahui adalah rumus dari
Jika benar untuk , maka ruas kiri menjadi ....
Pernyataan yang benar tentang momen inersia adalah ....
Suatu gas propana direaksikan dengan gas klorin dan dihasilkan senyawa X. Senyawa X yang dimaksud adalah ....
Jenis endositosis yang terjadi dimana sel "meneguk" tetesan fluida ekstraseluler dalam vesikula kecil disebut juga dengan ....
Himpunan penyelesaian dari persamaan trigonometri dengan adalah ....
Perhatikan tabel emisi karbon dioksida yang disebabkan berbagai pembangkit listrik berikut!
Sebuah kantor kecil di kawasan SCBD memiliki komputer sebanyak 10 unit, mesin fotokopi sebanyak 1 unit, dispenser sebanyak 2 unit, proyektor sebanyak 3 unit, dan AC sebanyak 4 unit. Konsumsi daya serta lama waktu pemakian rata-rata harian dari masing-masing peralatan kantor tersebut adalah
Diketahui bahwa kantor-kantor di kawasan SCBD disuplai oleh PLTU Muara Karang yang menggunakan batu bara jenis bituminous sebagai sumber energinya. Berapa besar kontribusi karbon dioksida yang dihasilkan oleh kantor tersebut setiap harinya?







