Bank Soal Kimia SMA Nilai pH Larutan Garam
Soal
LOTS Memahami
Soal Populer Hari Ini
Budi memiliki sebuah bambu sepanjang m. Karena terlalu panjang, bambu itu dipotong dan dibuang m . Panjang bambu itu sekarang adalah ...
Matematika
Level 5
Bilangan
Operasi Hitung Pecahan
Operasi Hitung Pecahan Biasa dan Campuran
Potensi wilayah Indonesia berdasarkan letak astronomis adalah ....
IPS
Level 5
Geografi
Karakteristik Geografi Wilayah Indonesia
Potensi Keadaan Geografis

Andi mengikuti lomba menulis cerpen dalam iklan tersebut. Jika Andi berhasil menjadi juara II, hadiah yang berhasil didapatkan Andi adalah sertifikat dan uang sebesar ....
Bahasa Indonesia
Level 5
Membaca
Iklan
Identifikasi Informasi
Read the text below. Then, fill in the blank with a correct verb to be.

Source: creazilla.com
My name is Claire. I live in Arizona. I am in fifth grade. I have a brother. His name is Peter. He is in fourth grade.
Based on the text, we know that Claire and Peter ... students.
Bahasa Inggris
Level 5
Bahasa Inggris
Friendship
Self-Introduction
Delapan buah tangki masing-masing berisi 500 liter air. Tangki tersebut dihubungkan dengan selang untuk dialirkan ke tambak udang. Setelah 10 menit, air di dalam tangki tersisa 2.500 liter. Berapa dm3/ menit debit air yang dialirkan?
Matematika
Level 5
Geometri
Perbandingan Dua Besaran
Debit
Perhatikan gambar berikut!
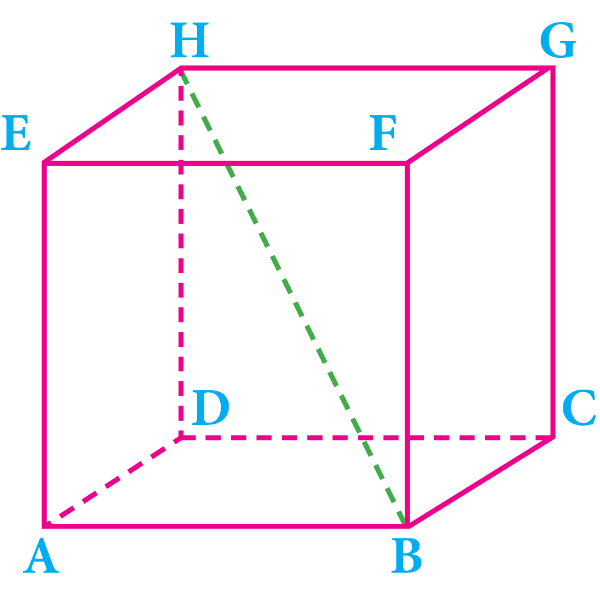
Garis hijau yang menghubungkan titik B dengan tittik H pada gambar kubus di atas disebut ....
Matematika
Level 5
Geometri
Balok dan Kubus
Sifat dan Jaring-Jaring Balok dan Kubus
Berikut adalah tabel dari hobi siswa-siswa kelas 6 SD Mulya.
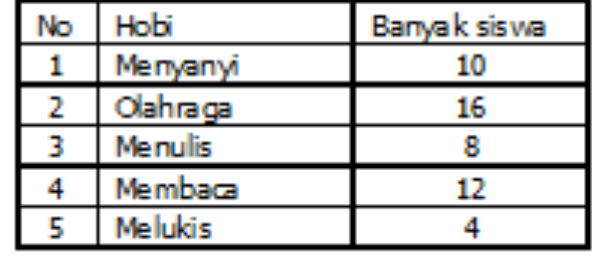
Diagram lingkaran yang tepat sesuai dengan data di atas adalah ....
Matematika
Level 5
Statistika
Pengumpulan dan Penyajian Data
Menyajikan Data
Bagian awal teks eksplanasi berupa ....
Bahasa Indonesia
Level 5
Membaca
Teks Eksplanasi
Struktur Teks Eksplanasi
Perhatikan diagram berikut!

Pernyataan yang sesuai dengan diagram di atas adalah ...
Matematika
Level 5
Statistika
Pengumpulan dan Penyajian Data
Membaca Data
Bacalah kutipan surat undangan berikut ini!
Dengan hormat,
Melalui surat ini, kami bermaksud mengundang Bapak/Ibu untuk hadir dalam acara pengambilan rapor semester ganjil untuk kelas I-VI tahun pelajaran 2019/2020. Acara tersebut akan dilaksanakan pada:
hari : Sabtu
tanggal : 7 Desember 2019
waktu : 09.00 WIB
tempat : Kelas masing-masing
Kami harap Bapak/Ibu dapat hadir tepat waktu. [...]
Kalimat efektif yang tepat untuk melengkapi kutipan surat undangan tersebut adalah ....
Bahasa Indonesia
Level 5
Membaca
Surat Undangan
Menulis Surat Undangan
Cek Contoh Kuis Online
Kejar Kuis
Cek Contoh Bank Soal
Kejar Soal
Budi memiliki sebuah bambu sepanjang m. Karena terlalu panjang, bambu itu dipotong dan dibuang m . Panjang bambu itu sekarang adalah ...
Potensi wilayah Indonesia berdasarkan letak astronomis adalah ....
Andi mengikuti lomba menulis cerpen dalam iklan tersebut. Jika Andi berhasil menjadi juara II, hadiah yang berhasil didapatkan Andi adalah sertifikat dan uang sebesar ....
Read the text below. Then, fill in the blank with a correct verb to be.

Source: creazilla.com
My name is Claire. I live in Arizona. I am in fifth grade. I have a brother. His name is Peter. He is in fourth grade.
Based on the text, we know that Claire and Peter ... students.
Delapan buah tangki masing-masing berisi 500 liter air. Tangki tersebut dihubungkan dengan selang untuk dialirkan ke tambak udang. Setelah 10 menit, air di dalam tangki tersisa 2.500 liter. Berapa dm3/ menit debit air yang dialirkan?
Perhatikan gambar berikut!
Garis hijau yang menghubungkan titik B dengan tittik H pada gambar kubus di atas disebut ....
Berikut adalah tabel dari hobi siswa-siswa kelas 6 SD Mulya.
Diagram lingkaran yang tepat sesuai dengan data di atas adalah ....
Bagian awal teks eksplanasi berupa ....
Perhatikan diagram berikut!
Pernyataan yang sesuai dengan diagram di atas adalah ...
Bacalah kutipan surat undangan berikut ini!
Dengan hormat,
Melalui surat ini, kami bermaksud mengundang Bapak/Ibu untuk hadir dalam acara pengambilan rapor semester ganjil untuk kelas I-VI tahun pelajaran 2019/2020. Acara tersebut akan dilaksanakan pada:
hari : Sabtu tanggal : 7 Desember 2019 waktu : 09.00 WIB tempat : Kelas masing-masing
Kami harap Bapak/Ibu dapat hadir tepat waktu. [...]
Kalimat efektif yang tepat untuk melengkapi kutipan surat undangan tersebut adalah ....







